
| A. | A的一种单质具有良好的导电性 | |
| B. | 氧化物对应水化物的酸性:D>A | |
| C. | B、C的单质均可与NaOH溶液反应生成氢气 | |
| D. | A、B、C三种元素均可以与D元素形成共价化合物 |
分析 B原子的电子层数与最外层电子数相等,可为Be或Al,D元素最高正价与最低负价的绝对值之差为6,应为Cl元素,A和C同主族,且四种元素质子的最外层电子数之和为18,如B为Be,则A、C的最外层电子数为$\frac{18-7-2}{2}$=4.5,不满足电子数为整数的特点,则B应为Al,A、C的最外层电子数为$\frac{18-7-3}{2}$=4,则A为C、C为Si元素,结合对应单质、化合物的性质以及元素周期率解答该题.
解答 解:由以上分析可知A为C、B为Al、C为Si、D为Cl元素.
A.A为C,如为石墨,则具有良好的导电性,故A正确;
B.如不是最高价氧化物的水化物,则酸性不一定强,如HClO的酸性比碳酸弱,故B错误;
C.Al、Si可与氢氧化钠溶液反应,生成气体为氢气,故C正确;
D.四氯化碳、氯化铝以及四氯化硅都为共价化合物,故D正确.
故选B.
点评 本题考查了原子结构与元素周期律的关系,为高考常见题型,题目难度不大,推断元素为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题有利于提高学生的分析能力及逻辑推理能力.


科目:高中化学 来源: 题型:选择题
| A. | 该反应是一个放热反应 | |
| B. | 参加反应的氢气和氧气的总能量高于反应生成的水的总能量 | |
| C. | 该反应是一个吸热反应 | |
| D. | 参加反应的氢气和氧气的总能量高于反应生成的水的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,1 LpH=l的硫酸溶液中,含有H+的数目为0.2NA | |
| B. | 1 mol Na2O2与水完全反应时转移电子数目为2 NA | |
| C. | 向含1 mol Cl-的NH4Cl溶液中加入氨水使溶液呈中性,此时溶液中NH4+数目为NA | |
| D. | 向2 mL0.5 mol/L硅酸钠溶液中滴入过量盐酸制硅酸胶体,所得胶粒数目为0.001 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
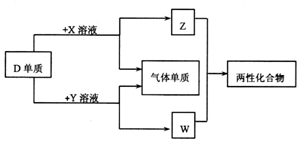 A、B、C、D、E为原子序数依次增大的短周期主族元素,分布在三个不同周期.X、Y、Z、W为这些元素形成的化合物,X为二元化合物且为强电解质,W的水溶液呈碱性,物质的转化关系如图所示.下列说法中正确的是( )
A、B、C、D、E为原子序数依次增大的短周期主族元素,分布在三个不同周期.X、Y、Z、W为这些元素形成的化合物,X为二元化合物且为强电解质,W的水溶液呈碱性,物质的转化关系如图所示.下列说法中正确的是( )| A. | 离子半径:C+>D3+>B2- | |
| B. | C的单质的熔点低于D的单质的熔点 | |
| C. | 电解C、E形成的化合物水溶液可生成C、E对应的单质 | |
| D. | 由A、B、E形成的化合物都含有共价键,溶液都呈强酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 其他条件不变时,改变密闭容器中某一条件,对反应A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所 示的曲线(T 表示温度,n 表示物质的量).下列判断正确的是( )
其他条件不变时,改变密闭容器中某一条件,对反应A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所 示的曲线(T 表示温度,n 表示物质的量).下列判断正确的是( )| A. | 若 T1>T2,则正反应是吸热反应 | |
| B. | 达到平衡时,A2转化率:b>a>c | |
| C. | 在 T2和起始 n(A2)不变时达到平衡,n(AB3)大小为:c>b>a | |
| D. | 若 T2>T1,达到平衡时 b、d 两点的反应速率为:d>b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +46 kJ/mol | B. | +92kJ/mol | C. | -46 kJ/mol | D. | -92 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料 | |
| B. | 利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用 | |
| C. | 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应 | |
| D. | 石英、玛瑙的主要成分是二氧化硅,陶瓷、分子筛主要成分是硅酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com