
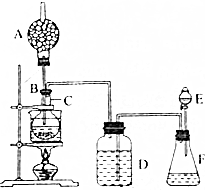
分析 将E中浓H2SO4滴入F中浓盐酸中,由于浓H2SO4有吸水性,且溶于水要放出大量的热,故F中逸出HCl(g),经D中浓H2SO4干燥,进入C中,HCl溶于C2H5OH中,二者发生反应:C2H5OH+HCl→C2H5Cl+H2O,CuSO4吸收水分变为蓝矾,促使上列反应向右进行,加热时,生成的C2H5Cl从A处逸出,点燃火焰呈绿色,以此解答该题.
解答 解:(1)浓盐酸在浓硫酸作用下,由于浓H2SO4有吸水性,且溶于水要放出大量的热,可促使盐酸的挥发,F中逸出的气体的主要成分是生成氯化氢气体,
故答案为:氯化氢;
(2)D中为浓硫酸,进入D中的气体为氯化氢,浓硫酸可起到吸收氯化氢气体中混有的水蒸气的作用,
故答案为:吸收氯化氢气体中混有的水蒸气;
(3)B导管较长,可起到冷凝回流的作用,故答案为:冷凝乙醇蒸气;
(4)点燃火焰呈绿色,说明A出燃烧的气体为CH3CH2Cl,故答案为:CH3CH2Cl;
(5)C瓶中无水硫酸铜变蓝,说明反应有水生成,即氯化氢与乙醇发生取代反应生成水,水与无色CuSO4粉末结合生成蓝色的CuSO4晶体,
故答案为:反应产物有H2O生成,水与无色CuSO4粉末结合生成蓝色的CuSO4晶体;
点评 本题考查物质的性质实验,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握实验的原理和操作注意事项,题目难度中等.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:选择题
| A. | 所得溶液中c(Cu2+)=0.225mol/L | |
| B. | 所得溶液中c(Cu2+)=0.03mol/L | |
| C. | 所得气体在标准状况下的体积为0.448L | |
| D. | 反应中转移0.06mol的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1项 | B. | 2项 | C. | 3项 | D. | 4项 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8 g苯含有碳碳双键的数目为0.3NA | |
| B. | 标准状况下,足量的Fe与2.24 L Cl2反应转移电子的数目为0.3NA | |
| C. | 1.6 g CH4含有共用电子对的数目为0.5NA | |
| D. | 100mLpH=2的新制氯水中,:N(OH-)+2N(ClO-)+N(HClO)=0.001NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.  .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

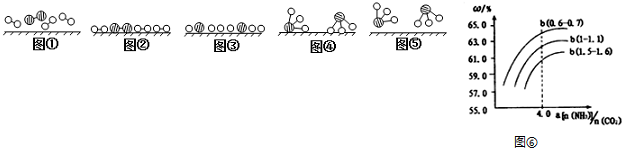
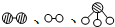 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中化学键断裂.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中化学键断裂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2和CH2=CH-CH=CH2 | B. | C4H8和C6H12 | ||
| C. | 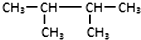 和(CH3)2CHCH(CH3)2 和(CH3)2CHCH(CH3)2 | D. | C2H6和C4H10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com