


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
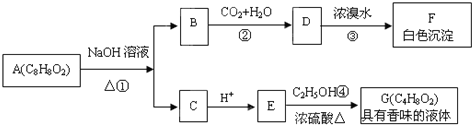
查看答案和解析>>
科目:高中化学 来源: 题型:
| 用途 | 解释 | |
| A | SO2可用于漂白纸浆 | SO2具有氧化性 |
| B | 明矾可用于净水 | 明矾在水中生成的氢氧化铝胶体有吸附性 |
| C | 纯碱可去油污 | 纯碱水解呈碱性 |
| D | “84”消毒液可用于漂白 | 置于空气中生成的次氯酸有氧化性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只含有一种元素的物质一定是单质 |
| B、胶体与溶液的本质区别在于是否有丁达尔现象 |
| C、一定温度、压强下,气体体积由其物质的量的多少决定 |
| D、向盛有沸水的烧杯中滴加FeCl3溶液并长时间煮沸,制备Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,0.1 mol/L HF溶液pH=1 |
| B、Ksp(CaF2)随温度和浓度的变化而变化 |
| C、向反应后的溶液中继续加入100m L 0.1 mol/L Na2CO3有CaCO3沉淀产生 |
| D、该体系中有CaF2沉淀产生,且反应后溶液中的F-浓度为1×10-4.5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液退色 |
| B、乙酸与乙醇可以发生酯化反应,又均可与氢氧化钠溶液反应 |
| C、糖类、油脂和蛋白质在一定条件下都能发生水解反应 |
| D、工业上通过石油分馏可以得到多种轻质液体燃料,通过煤的干馏可获得焦炭、煤焦油、焦炉气等多种化工原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| 加热、加压 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com