
【题目】在密闭容器中进行如下反应:CO2(g)+C(s)![]() 2CO(g) ΔH>0,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
2CO(g) ΔH>0,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
(1)增加C,平衡_________(填“正向移动”、“逆向移动”或“不移动”,下同),c(CO2)__________(填“增大”、“减小”或“不变”,下同)。
(2)缩小反应容器的容积,保持温度不变,则平衡__________________,c(CO2)__________________。
(3)保持反应容器的容积和温度不变,通入N2,则平衡_________________,c(CO2)__________________。
(4)保持反应容器的容积不变,升高温度,则平衡__________________,c(CO)__________________。
科目:高中化学 来源: 题型:
【题目】如图所示电化学装置,X可能为“锌棒”或“碳棒”,下列叙述错误的是

A.X为锌棒,仅闭合K1,Fe电极上发生还原反应
B.X为锌棒,仅闭合K1,产生微量电流方向:Fe→X
C.X为碳棒,仅闭合K2,该电化学保护法称为“牺牲阳极阴极保护法”
D.若X为碳棒,仅闭合K1,铁电极的极反应为:Fe -2e- → Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,下列说法正确的是

A. Z单质的化学活泼性一定比Y单质的强
B. W的原子序数可能是Y的原子序数的2倍
C. W的气态氢化物的稳定性一定比Y的强
D. X和W两元素不可能形成共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇的主要反应如下:
①CO(g)+2H2(g) ![]() CH3OH(g) ΔH1<0
CH3OH(g) ΔH1<0
②CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH2<0
CH3OH(g)+H2O(g) ΔH2<0
③CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH3>0
CO(g)+H2O(g) ΔH3>0
回答下列问题:
(1)反应①的化学平衡常数K表达式为___________________;图1中能正确反映平衡常数K随温度变化关系的曲线为_______(填曲线标记字母),其判断理由是______________________。
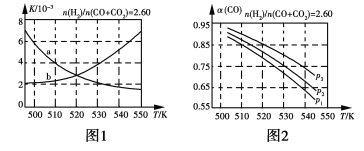
(2)合成气组成n(H2)/n(CO+CO2)=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而___________(填“增大”或“减小”),其原因是___________________;图2中的压强由大到小为_________________________,其判断理由是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 氯化钙溶液中通入CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+
B. 以石墨作电极电解氯化铝溶液:2Cl–+2H2O电解2OH–+H2↑+Cl2↑
C. 200 mL 2 mol/L的FeBr2溶液中通入11.2 L标准状况下的氯气:4Fe2++6Br–+5Cl2=4Fe3++3Br2+10Cl–
D. 向明矾溶液中加人氢氧化钡溶液至沉淀的物质的量最大:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com