
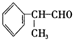
 是一种重要的化工原料,其合成路线如下:
是一种重要的化工原料,其合成路线如下: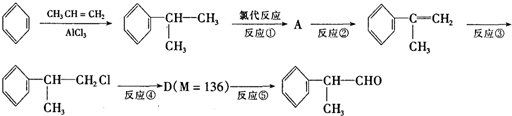
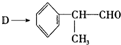 反应的化学方程式为
反应的化学方程式为 的结构可知,苯和CH3CH=CH2在AlCl3作用下发生加成反应生成
的结构可知,苯和CH3CH=CH2在AlCl3作用下发生加成反应生成 ,与氯气发生取代反应生成氯代烃,结合转化关系可知A为
,与氯气发生取代反应生成氯代烃,结合转化关系可知A为 ,由
,由 结构可知反应②为消去反应,反应③
结构可知反应②为消去反应,反应③ 生成
生成 ,C=C键变为C-C键,为
,C=C键变为C-C键,为 与HCl发生加成反应,D的相对分子质量为136,D在催化剂作用下可被氧化为
与HCl发生加成反应,D的相对分子质量为136,D在催化剂作用下可被氧化为 ,说明D中含有-OH,可被氧化,则D应为
,说明D中含有-OH,可被氧化,则D应为 ,则反应④为
,则反应④为 在NaOH水溶液、加热条件下的水解反应生成醇,结合有机物的官能团以及题目要求解答该题.
在NaOH水溶液、加热条件下的水解反应生成醇,结合有机物的官能团以及题目要求解答该题. 含有-CHO,可被氧化为-COOH,为羧基,故答案为:羧基;
含有-CHO,可被氧化为-COOH,为羧基,故答案为:羧基; 结构可知反应②为消去反应,反应③
结构可知反应②为消去反应,反应③ 生成
生成 ,C=C键变为C-C键,为
,C=C键变为C-C键,为 与HCl发生加成反应,故答案为:消去反应;加成反应;
与HCl发生加成反应,故答案为:消去反应;加成反应; 在NaOH水溶液、加热条件下的水解反应生成
在NaOH水溶液、加热条件下的水解反应生成 ,故答案为:NaOH水溶液、加热;
,故答案为:NaOH水溶液、加热; ,D中含有-OH,可被氧化,生成
,D中含有-OH,可被氧化,生成 ,反应的化学方程式为
,反应的化学方程式为 ,故答案为:
,故答案为: ;
; ,相对分子质量为136,与有机物X在一定条件下可生成一种相对分子质量为178的酯类物质,设X的相对分子质量为M(X),则有M(
,相对分子质量为136,与有机物X在一定条件下可生成一种相对分子质量为178的酯类物质,设X的相对分子质量为M(X),则有M( )+M(X)=178+M(H2O),M(X)=60,应为CH3COOH,D有多种同分异构体,能满足苯环上有两个取代基,且能使FeCl3溶液显紫色,说明含有酚羟基,则同分异构体有-CH2CH2CH3和-CH(CH3)2对应的有机物,各有邻、间、对三种,共6种,故答案为:CH3COOH;6.
)+M(X)=178+M(H2O),M(X)=60,应为CH3COOH,D有多种同分异构体,能满足苯环上有两个取代基,且能使FeCl3溶液显紫色,说明含有酚羟基,则同分异构体有-CH2CH2CH3和-CH(CH3)2对应的有机物,各有邻、间、对三种,共6种,故答案为:CH3COOH;6.


科目:高中化学 来源: 题型:

| A、图①表示可逆反应CO(g)+H20(g)?5C02 (g)+H2(g)△H>0 |
| B、图②表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)影响,乙的压强大 |
| C、图③表示有无催化剂化学反应中能量变化 |
| D、图④表示C02通人饱和碳酸钠溶液中,溶液导电性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 操 作 | 结 论 | |
| 甲 | 分别滴在火柴梗上 | 变黑者为浓硫酸 |
| 乙 | 分别加入金属铝片 | 产生刺激性气味者为浓硫酸 |
| 丙 | 分别加入到盛水的试管中 | 放热很显著的为浓硫酸 |
| 丁 | 分别用玻璃棒蘸浓氨水靠近盛酸的瓶口 | 冒白烟的为浓硫酸 |
| 戊 | 分别加到CuSO4?5H2O 晶体中 | 变白者为浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:

 制成,合成路线如下:
制成,合成路线如下:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、n:( n+2 ) |
| B、1:1 |
| C、1:( n+2 ) |
| D、(n+2):n |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、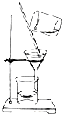 用如图所示装置除去Fe(OH)3胶体中含有的少量FeCl3杂质 |
B、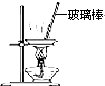 用如图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
C、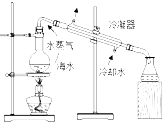 用如图所示装置从海水制取蒸馏水 |
D、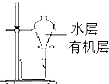 用如图所示装置分离酒精萃取碘水中的碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+)>c(OH-)的任意水溶液 |
| B、加酚酞后显无色的溶液 |
| C、pH=6的某溶液 |
| D、能与金属Al反应放出H2的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com