
【题目】甲苯氧化法制备苯甲酸的反应原理如下:
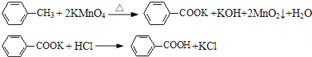
实验时将一定量的甲苯和KMnO4溶液置于图装置中,在100 ℃时,反应一段时间,再停止反应,并按如下流程分离出苯甲酸和回收未反应的甲苯。
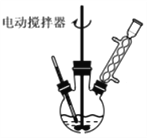
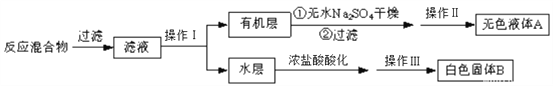
(1)反应图示装置中,冷凝管的作用是________。
(2)实验室中实现操作I所需的玻璃仪器有_________,烧杯;操作II的名称为_______。
(3)如果操作I后的水层呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,否则会出现的危害是______。
(4)分离出的苯甲酸中若混有少量氯化钾,进一步提纯应采用的操作方法是_______(填名称)。
(5)纯度测定:称取1.220g产品,配成100mL溶液,取其中25.00mL溶液,进行滴定,消耗KOH物质的量为2.4×10-3mol。产品中苯甲酸质量分数为_____。
【答案】 冷凝回流,提高原料利用率 分液漏斗 蒸馏 过量的高锰酸钾氧化盐酸,产生氯气 重结晶 96%
【解析】(1)冷凝管的作用是冷凝回流,提高原料利用率;(2)操作I为分液操作,其所需的玻璃仪器有分液漏斗、烧杯;操作II为蒸馏操作得无色液体A;(3)为了避免过量的高锰酸钾氧化盐酸,产生有毒的氯气,应该先加亚硫酸氢钾除去过量的高锰酸钾,然后再加入浓盐酸酸化;(4)分离出的苯甲酸中若混有少量氯化钾,利用两者的溶解度差,进一步提纯应采用的操作方法是重结晶;(5) c(KOH)=![]() =0.0096 mol·L-1;1L溶液中含KOH的物质的量为0.0096 mol·L-1×1 L=0.0096 mol,在0.56 g苛性钾样品中含KOH的质量为:0.0096 mol×56 g·mol-1=0.5376g,苛性钾的纯度=
=0.0096 mol·L-1;1L溶液中含KOH的物质的量为0.0096 mol·L-1×1 L=0.0096 mol,在0.56 g苛性钾样品中含KOH的质量为:0.0096 mol×56 g·mol-1=0.5376g,苛性钾的纯度=![]() ×100%=96%。
×100%=96%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A、E在元素周期表中的相对位置如图所示,A与氧元素能形成两种无色气体,C是地壳中含量最多的元素,D是地壳中含量最多的金属元素。

(1)C在元素周期表中的位置为________,其简单离子的结构示意图为________________。
(2)AE2的分子式为__________。
(3)C、D、E、F的离子半径由大到小的顺序是___________(填离子符号)。
(4)实验室制取F的单质气体的离子方程式为________________________。
(5)在微电子工业中,B的简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备高纯硅有多种方法,其中的一种工艺流程如下:
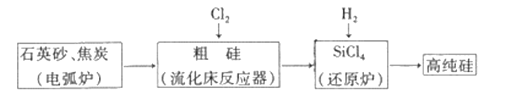
已知:流化床反应的产物中,除SiCl4外,还有SiHCl3、SiH2Cl2、SiH3Cl、FeCl3等。下列说法正确的是
A. 电弧炉中发生的反应为C+SiO2![]() CO2↑+Si
CO2↑+Si
B. SiCl4进入还原炉之前需要经过蒸馏提纯
C. 每生产l mol高纯硅,需要44. 8L Cl2(标准状况)
D. 该工艺Si的产率高,符合绿色化学要求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某阳离子Mn+的核外共有x个电子,核内有a个中子,则M的质量数为 ( )
A. a+x-n B. a-x+n
C. a-x-n D. .a+x+n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备无水乙醇常用蒸馏法,实验步骤如下:
I.回流:在l00mL圆底烧瓶中加入l0g小颗粒状的生石灰和几颗氢氧化钠,慢慢注入50mL工业乙醇,回流1h。
Ⅱ.蒸馏:回流毕,待烧瓶冷却后在烧瓶中加入几粒沸石,改为蒸馏装置,收集78C时的馏分,即为无水乙醇。回流和蒸馏装置如下图(用△表示酒精灯):
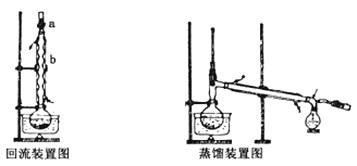
回答下面问题:
(1)装置b的名称是________ 。
(2)简述向烧瓶中加入生石灰的方法_____________
(3)加入NaOH固体是为了除去工业乙醇中少量的醛,发生的关键反应为CH3CHO+CH3CHO![]() CH3CH(OH)CH2CHO,该反应的反应类型为____,回流1h的目的是___ 。
CH3CH(OH)CH2CHO,该反应的反应类型为____,回流1h的目的是___ 。
(4)蒸馏时,先____,后____(①点燃酒精灯②接通冷凝水,填代号),待温度计指示为78℃左右时,尾接管中出现液滴,弃去开始流出的液体,原因是____。
(5)有同学建议改蒸馏为过滤,请回答过滤法不妥的原因 ___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,浓硫酸既表现为强氧化性,又表现为酸性的是( )
A. 2NaCl(s)+H2SO4(浓)=Na2SO4+2HCl↑
B. C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O
C. Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
D. Na2CO3+H2SO4(浓)=Na2SO4+H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.向Na2CO3溶液中逐滴加入HCl,直到不再生成CO2气体为止,在此过程中.溶液中的HCO3-浓度变化是先变大后变小(溶液体积变化均忽略不计)
B.向NaHCO3溶液中加入Ba(OH)2固体,CO32-的浓度变化是先变大后变小(溶液体积变化均忽略不计)
C.有含0.2molNa2CO3和含0.3molHCl的两种溶液:①将Na2CO3溶液逐滴滴入HCl溶液中;②将HCl溶液逐滴滴入Na2CO3溶液中,①②两种操作生成的CO2体积之比为3:2
D.将等质量的Na2O和Na2O2样品分别放入等量的水中,所得溶液的质量分数分别为a%和b%,则a、b的关系是a=b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某燃煤发电厂处理废气的装置示意图.下列说法正确的是( )

A. 此过程中没有分解反应
B. 整个过程的反应可表示为: 2SO2+2CaCO3+O2═2CaSO4+2CO2
C. 使用此废气处理装置可减少CO2的排放
D. 此过程中S元素的化合价未发生改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com