
| A. | Li Na K | B. | Ba2+ Ca2+ Mg2+ | C. | Cl-K+ Ca2+ | D. | N O F |
分析 A.同主族自上而下原子半径增大;
B.离子电子层越多,离子半径越大;
C.离子电子层结构相同,核电荷数越大离子半径越大;
D.同周期自左而右原子半径减小.
解答 解:A.同主族自上而下原子半径增大,则原子半径大小为:Li<Na<K,故A正确;
B.离子电子层越多,离子半径越大,则离子半径大小为:Ba2+>Ca2+>Mg2+,故B错误;
C.离子电子层结构相同,核电荷数越大离子半径越小,则离子半径大小为:Ca2+<K+<Cl-,故C错误;
D.同周期自左而右原子半径减小,则原子半径大小顺序为:N>O>F,故D错误.
故选A.
点评 本题考查了微粒半径大小比较,题目难度不大,明确粒子半径与电子层数、核电荷数的关系为解答关键,注意判断微粒半径时首先比较电子层数,电子层相同时再比较核电荷数.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:选择题
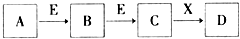 中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去).下列推断不正确的是( )
中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去).下列推断不正确的是( )| A. | 若D是一种强碱,则A、B、C均可与X反应生成D | |
| B. | 若D为NaCl,且A可与C反应生成B,则E可能是CO2 | |
| C. | 若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁 | |
| D. | 若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通常情况下,32gO2和O3的混合气体含有的分子总数小于NA | |
| B. | 常温常压下,0.1mol•L-1的硝酸铵溶液中氮原子数目为0.2NA | |
| C. | 1mol有机物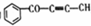 中最多有6NA个原子在一条直线上 中最多有6NA个原子在一条直线上 | |
| D. | 1mol甲基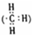 所含的电子数为7NA 所含的电子数为7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
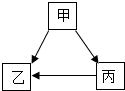 无机物甲、乙、丙经一步反应的转化关系如图所示,其中部分反应物、生成物及反应条件已略去.
无机物甲、乙、丙经一步反应的转化关系如图所示,其中部分反应物、生成物及反应条件已略去.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大反应物浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多 | |
| B. | 有气体参加的化学反应,增大压强(缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大 | |
| C. | 升高温度能使化学反应速率增大的主要原因是增加了反应物分子中活化分子的百分数 | |
| D. | 催化剂能增大单位体积内活化分子的百分数,从而成千上万倍地增大化学反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 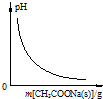 图表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化 | |
| B. | 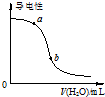 图表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b | |
| C. | 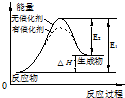 图表示催化剂能改变化学反应的焓变 | |
| D. | 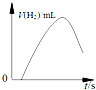 图表示表面有氧化膜的镁条投入稀盐酸中产生氢气的速率随时间的变化曲线 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com