
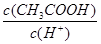 ④
④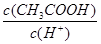 ⑤c(OH-) ⑥c(CH3COO-)
⑤c(OH-) ⑥c(CH3COO-)| A.①②③ | B.②③⑤ | C.④⑤ | D.④⑤⑥ |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.HF的电离平衡常数为7.2×10-4 |
| B.HNO2的电离平衡常数为4.9×10-10 |
| C.根据①③两个反应即可知三种酸的相对强弱 |
| D.HNO2的电离平衡常数比HCN大,比HF小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②⑥⑦ | B.③④⑥⑦ | C.③④⑤⑥ | D.①② |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.水电离出的c(H+):③>①>② |
| B.溶液的pH:②>③>① |
| C.①和②等体积混合后的溶液:c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) |
| D.①和③等体积混合后的溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(NH4+):③>① |
| B.水电离出的c(H+):②>① |
| C.①和②等体积混合后的溶液:c(H+)=c(OH-)+c(NH3·H2O) |
| D.①和③等体积混合后的溶液:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
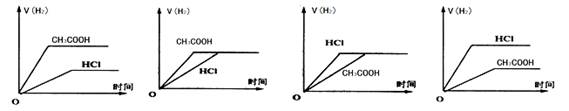
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 酸 | 电离常数 |
| 碳酸 | K1=4×10-7 K2=5.6×10-11 |
| 亚硫酸 | K1=1.54×10-2 K2=1.02×10-7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(CH3COOH)=0.01mol·L-1 |
| B.c(H+)=c(CH3COO-) |
| C.加水稀释100倍后,溶液pH=4 |
| D.加入醋酸钠固体,可抑制醋酸的电离 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.60℃时,NaCl溶液的pH<7,则溶液呈酸性 |
| B.将pH=4的CH3COOH溶液加水稀释,溶液中所有离子的浓度均减小 |
| C.常温下,CH3COOH分子可能存在于pH>7的碱性溶液中 |
| D.相同温度下,1 mol·L-1氨水与0.5 mol·L-1氨水中c(OH-)之比是2∶1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com