
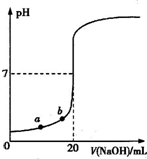
| A.水电离出的氢离子浓度:a>b |
| B.盐酸的物质的量浓度为0.0100mol?L-1?? |
| C.指示剂变色时,说明盐酸与NaOH恰好完全反应 |
| D.当滴加NaOH溶液10.00 mL(忽略反应前后体积变化),该混合液的pH=1+lg3 |
| 0.02L×0.1mol/L-0.01L×0.1mol/L |
| 0.03L |
| 1 |
| 3 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.M点所示溶液导电能力强于Q点 |
| B.N点所示溶液中c(CH3COO-)>c(Na+) |
| C.M点和N点所示溶液中水的电离程度相同 |
| D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.(c)(a)(b)(d)(f)(e)(g) | B.(c)(a)(d)(f)(b)(e)(g) | C.(g)(e)(b)(f)(d)(a)(c) | D.(c)(a)(d)(f)(e)(b)(g) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用氢氧化钠溶液滴定食醋,开始时溶液的pH通常变化缓慢,当接近完全反应时(即滴定终点),pH出现突变,称为滴定突跃 |
| B.硝酸钾饱和溶液冷却未出现结晶时,可以用玻璃棒充分磨擦器皿壁促使晶体析出 |
| C.抽滤装置由布氏漏斗、吸滤瓶、安全瓶、抽气泵等仪器组成,工作的主要原理是抽气泵给吸滤瓶减压,导致装置内部的压强降低,使过滤的速度加快 |
| D.Cu2+与过量氨水反应制取Cu(0H)2,离子方程式为Cu2++2NH3?H20═Cu(OH)2↓+2NH4+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
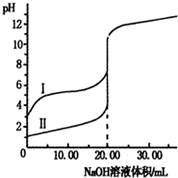
| A.I、Ⅱ分别表示盐酸和醋酸的滴定曲线 |
| B.盐酸和醋酸的浓度均为0.1000mol?L-1 |
| C.pH=7时,两种酸所消耗NaOH溶液的体积相等 |
| D.V(NaOH)=20.00mL时,c(Cl-)=c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NO:0.001mol?L-1 | B.H2O:0.002mol?L-1 |
| C.NH3:0.002mol?L-1 | D.O2:0.0025mol?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com