
| A. | x=10时,溶液中有NH4+、Al3+、SO42-,且c(NH4+)=c(Al3+) | |
| B. | x=20时,溶液中所发生的反应离子方程式为:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| C. | x=30时,溶液中有Ba2+、AlO2-、OH-,且c(OH-)>c(AlO2-) | |
| D. | 滴加过程中,生成沉淀的最大物质的量为0.003mol |
分析 当x=10时,NH4Al(SO4)2与Ba(OH)2等物质的量反应,此时OH-量不足,OH-先与Al3+反应,与NH4+不反应,所以溶液中有没有参加反应的NH4+和部分剩余的Al3+存在,同时SO42-也有剩余,但此时不会有AlO2-生成,结合铵根离子水解解答;当x=30时,0.001 mol的NH4Al(SO4)2与0.003 mol Ba(OH)2反应,生成0.002 mol BaSO4、0.001 mol NaAlO2、0.001 mol NH3•H2O,且剩余0.001 mol Ba2+和0.001 mol OH-,由于NH3•H2O也是一种碱,存在电离平衡:NH3•H2O?NH4++OH-,据此判断反应中c(OH-)与c(AlO2-)、c(Ba2+)的大小关系.
解答 解:A、当x=10时,NH4Al(SO4)2与Ba(OH)2等物质的量反应,此时OH-量不足,OH-首先与Al3+反应,与NH4+不反应,所以溶液中有未参加反应的NH4+和部分剩余的Al3+存在,同时SO42-也有剩余,但此时不会有AlO2-生成,溶液中c(NH4+)>c(Al3+),故A错误;
B、x=20时,溶液中所发生的反应离子方程式为:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O,故B错误;
C、当x=30时,10ml0.1mol/LNH4Al(SO4)2溶液中含有0.001molNH4+,0.001molAl3+,0.002molSO42-,30ml等浓度Ba(OH)2溶液有0.003molBa2+,6mmolOH-,混合后硫酸钡沉淀,剩余0.001molBa2+;OH-过量溶液中存在0.001moAlO2-,铵根离子和氢氧根离子反应生成一水合氨,氢氧根离子剩余0.001mol;一水合氨电离生成铵根离子和氢氧根离子,此时c(OH-)>c(AlO2-),故C正确;
D、滴加过程中,生成沉淀的最大物质的量为氢氧化铝和硫酸钡沉淀,当 NH4Al(SO4)2溶液和Ba(OH)2溶液按照物质的量之比是1:2混合,沉淀的量最大,为0.002mol硫酸钡和0.001mol氢氧化铝,即沉淀的最大量是0.003mol,故D正确.
故选CD.
点评 本题考查了离子方程式的书写原则和方法应用,主要是定量反应的产物判断,关键分析离子反应顺序,先沉淀后反应生成弱电解质后沉淀溶解.


 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锗酸(化学式为H4GeO4),是难溶于水的弱酸 | |
| B. | ①硫酸比次氯酸稳定;②S2-易被氯气氧化,均能说明氯元素的非金属性比硫元素强 | |
| C. | 中学教材所附周期表中第15列元素的最高价氧化物对应水化物的化学式均为H3RO4 | |
| D. | HF的沸点比HCl 高,是因为H-F键比H-Cl键强 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CO在平衡时转化率为10% | |
| B. | 平衡浓度c(CO2)=c(H2) | |
| C. | 其他条件不变时,缩小体积,反应②平衡不移动 | |
| D. | 平衡时增大碳的质量,反应①中热量值不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠在空气中加热,生成淡黄色固体:2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2 | |
| B. | 向硫酸铝溶液中加入氨水制备氢氧化铝:Al3++3NH3•H2O═Al(OH)3 ↓+3NH4+ | |
| C. | 铁在潮湿的环境中生锈:3Fe+4H2O═Fe3O4+4H2↑ | |
| D. | 二氧化氮溶于水有硝酸生成:3NO2 +H2O═2HNO3+NO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应速率主要取决于②的快慢 | B. | NOBr2是该反应的催化剂 | ||
| C. | 该反应的焓变等于akJ•mol-1 | D. | 反应速率:v(NO)=v(NOBr)=2v(Br2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种元素的原子半径:r(Z)>r(X)>r(Y)>r(W) | |
| B. | X、Y、Z、W形成的单质最多有6种 | |
| C. | 四种元素均可与氢元素形成18电子分子 | |
| D. | 四种元素中.Z的最高价氧化物对应水化物酸化最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
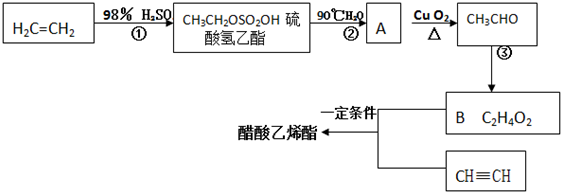
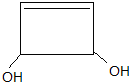 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com