
| A. | 2 L溶液中Ba2+和Cl-的总数为0.8NA | |
| B. | 500 mL溶液中Cl-的浓度为0.2 mol•L-1 | |
| C. | 500 mL溶液中Ba2+的浓度为0.2 mol•L-1 | |
| D. | 500 mL溶液中Cl-的总数为0.2NA |
分析 A.依据n=CV计算氯化钡的物质的量,氯化钡为强电解质,1mol氯化钡全电离产生1mol钡离子和2mol氯离子;
B.氯化钡溶液中氯离子浓度为氯化钡浓度2倍,结合溶液的均一性解答;
C.氯化钡溶液中钡离子浓度等于氯化钡浓度,结合溶液的均一性解答;
D.依据n=CV计算氯化钡的物质的量,氯化钡为强电解质,1mol氯化钡含有2mol氯离子,据此计算离子数目.
解答 解:A.2L0.2mol•L-1的BaCl2溶液含有氯化钡物质的量为0.4mol,含有钡离子和氯离子物质的量为:0.4+0.8=1.2mol,个数为1.2NA,故A错误;
B.0.2mol•L-1的BaCl2溶液,氯离子物质的量浓度为0.2mol/L×2=0.4mol/L,溶液的均一性,与体积无关,所以500 mL溶液中Cl-的浓度为0.4 mol•L-1,故B错误;
C.0.2mol•L-1的BaCl2溶液,钡离子浓度等于氯化钡溶液为0.2mol/L,溶液的均一性,与体积无关,所以500 mL溶液中Ba2+的浓度为0.2 mol•L-1,故C正确;
D.0.2mol•L-1的BaCl2溶液500 mL,含有氯化钡物质的量为0.2mol/L×0.5L=0.1mol,含有氯离子物质的量为0.2mol,个数为0.2NA,故D正确;
故选:AB.
点评 本题考查了物质的量浓度有关计算,明确物质的量浓度概念及计算公式,熟悉电解质与离子物质的量浓度之间关系是解题关键,题目难度不大.


 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 干冰只能用于人工降雨 | |
| B. | Al(OH)3可以治疗胃酸过多,因此可大量使用 | |
| C. | 为了增强去污效果,在洗衣粉中添加三聚磷酸钠(Na5P3O10) | |
| D. | 侯氏制碱法不涉及基本反应类型中的置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2 L HF中含有分子的数目为0.5 NA | |
| B. | 0.1 mol Fe与少量氯气反应生成FeCl2,转移电子数为0.2 NA | |
| C. | 1.4 g由乙烯和环丙烷组成的混合物中含有原子的数目为 0.3 NA | |
| D. | 0.1 mol•L-1碳酸钠溶液中含有CO32-离子数目小于0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅胶多孔,常用作食品干燥剂和催化剂的载体 | |
| B. | 汽车尾气中含有氮的氧化物,是汽油不完全燃烧造成的 | |
| C. | 服用阿司匹林出现水杨酸反应时,可以用NaHCO3溶液解毒 | |
| D. | 水玻璃可用作黏合剂和防火剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向上述溶液中滴加几滴NaOH溶液,溶液颜色会加深,因为OH-与Fe3+生成了红褐色沉淀 | |
| B. | 向上述溶液中滴加几滴NaOH溶液,溶液颜色会变浅,因为OH-与Fe3+生成了红褐色沉淀,使Fe3+的浓度减小,平衡逆向移动,导致Fe(SCN)3的浓度减小 | |
| C. | 向上述溶液中滴加几滴1 mol/L KSCN溶液,溶液颜色会加深,因为SCN-的浓度增大,正反应速率加快,平衡正向移动,导致导致Fe(SCN)3的浓度增大 | |
| D. | 向上述溶液中分别滴加NaOH溶液和KSCN溶液过程中,Na+、K+的浓度大小对平衡体系没有影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 不慎碰翻燃着的酒精灯使酒精在桌面上燃烧起来,应立即用湿抺布灭火 | |
| B. | 不慎将酸沾到皮肤或衣物上,应立即用浓NaOH溶液清洗 | |
| C. | 夜间厨房发生煤气泄漏时,立即开灯检查煤气泄漏原因,并打开所有门窗通风 | |
| D. | 用氢气还原氧化铜时,先加热氧化铜,再通入氢气 | |
| E. | 可燃性气体点燃前一定要验纯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
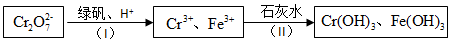
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 二氧化碳 | 碳酸钠 | 转移的电子 |
| A | lmol | 2NA | |
| B | 22.4L | lmol | |
| C | 106g | lmol | |
| D | 106g | 2NA |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com