
| 选项 | 实验目的 | 选用试剂或条件 | 解释 |
| A | 鉴别SO2和CO2 | 溴水 | 利用SO2的漂白性 |
| B | 鉴别Fe3+和Fe2+ | KSCN | 利用Fe3+的氧化性 |
| C | 鉴别硝酸钾和碳酸钠溶液 | 酚酞 | 碳酸钠溶液显碱性 |
| D | 鉴别食盐和氯化铵 | 加热 | 利用熔点不同 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二氧化硫与溴水发生氧化还原反应,二氧化硫表现还原性;
B.铁离子与硫氰根离子发生络合反应,不是氧化还原反应;
C.硝酸钾为强酸强碱盐,不水解,而碳酸钠为强碱弱酸盐,碳酸根离子水解溶液呈碱性;
D.氯化铵加热分解,而氯化钠较稳定.
解答 解:A.二氧化硅被溴水氧化,利用的是SO2的还原性,不是漂白性,故A错误;
B.铁离子与硫氰根离子结合生成络合物硫氰化铁,可用KSCN溶液鉴别鉴别Fe3+和Fe2+,利用的不是Fe3+的氧化性,故B错误;
C.硝酸钾溶液呈中性,碳酸钠溶液中碳酸根离子水解溶液呈碱性,可用酚酞鉴别硝酸钾和碳酸钠溶液,故C正确;
D.通过加热鉴别食盐和氯化铵,利用的是二者的稳定性,与熔点无关,故D错误;
故选C.
点评 本题考查化学实验方案的评价,题目难度不大,明确常见物质组成及性质为解答关键,注意掌握常见物质检验与鉴别方法,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:实验题
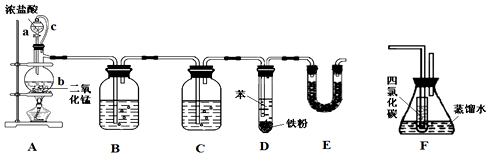
| 密度/g•cm-3 | 沸点/℃ | 水中溶解性 | |
| 苯 | 0.879 | 80.1 | 微溶 |
| 氯苯 | 1.11 | 131.7 | 不溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,74g乙酸甲酯中含共用电子对数为11NA | |
| B. | 1mol Cl2通入足量的水中,转移电子数为NA | |
| C. | 足量的铁粉与200mL1 mol•L-1硝酸完全反应生成H2的分子败为0.1NA | |
| D. | 30g葡萄糖和乙酸的混合物中含碳原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第一电离能:Y小于X | |
| B. | 气态氢化物的稳定性:Y大于X | |
| C. | 最高价含氧酸的酸性:X强于Y | |
| D. | X和Y形成化合物时,X显负价,Y显正价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用除去表面氧化膜的细铝条紧紧缠绕在温度计上(如图),将少许硝酸汞溶液滴到铝条表面,置于空气中,很快铝条表面产生“白毛”,且温度明显上升.下列分析错误的是( )
用除去表面氧化膜的细铝条紧紧缠绕在温度计上(如图),将少许硝酸汞溶液滴到铝条表面,置于空气中,很快铝条表面产生“白毛”,且温度明显上升.下列分析错误的是( )| A. | Al和O2化合放出热量 | B. | 硝酸汞是催化剂 | ||
| C. | 涉及了:2Al+3Hg2+→2Al3++3Hg | D. | “白毛”是氧化铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高炉炼铁时,增加炉高,可以改变尾气中一氧化碳的含量 | |
| B. | 厨房中燃气泄漏,立即打开抽油烟机排气 | |
| C. | “地沟油”禁止食用,但处理后可用来制肥皂和生物柴油 | |
| D. | 食盐中加碘单质可以减少碘缺乏症 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,向1L 0.1mo1•L-1NH4C1溶液中,不断加入固体NaOH后,NH4+与NH3•H2O的浓度变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是( )
常温下,向1L 0.1mo1•L-1NH4C1溶液中,不断加入固体NaOH后,NH4+与NH3•H2O的浓度变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是( )| A. | M点溶液中水的电离程度比原溶液大 | |
| B. | 随着NaOH的加入,NH4+与NH3•H2O物质的量总量减少 | |
| C. | 当n(NaOH)=0.05mol时,溶液中有:c(C1-)>c(Na+>c(NH4+>c(OH-)>c(H+) | |
| D. | 在M点时,n(OH-)+0.05═a+n(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
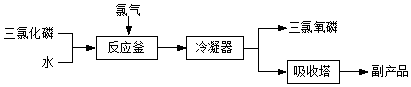
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
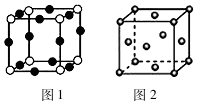 A、B、C、D、E是元素周期表中前36号元素,核电荷数依次增大,A与B能形成种类繁多的化合物,D原子中成对电子数等于未成对电子数的3倍;E+中所有电子正好充满K、L、M三个电子层.
A、B、C、D、E是元素周期表中前36号元素,核电荷数依次增大,A与B能形成种类繁多的化合物,D原子中成对电子数等于未成对电子数的3倍;E+中所有电子正好充满K、L、M三个电子层.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com