
| A.硫酸铵 | B.磷酸二氢钙 | C.硫酸钾 | D.尿素 |

科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.联合制碱法的优点是减少了对设备的腐蚀 |
| B.工业生产硫酸时,用98%硫酸的来吸收三氧化硫,可以避免形成酸雾并提高吸收率 |
| C.合成氨是天然固氮的方法之一 |
| D.碳酸钠俗称小苏打,甲烷是一种清洁能源 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.FeSO4·7H2O是常用的混凝剂,它除去悬浮固体颗粒的过程只是物理过程 |
| B.用纯碱和生石灰处理硬水,既可以除去暂时硬度,也可以除去永久硬度 |
| C.永久硬度的水可以采用离子交换法进行软化,其主要就是利用了离子交换膜技术 |
| D.污水处理中的三级处理是采用化学方法,对污水进行深度处理和净化 |
 渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.上述生产过程中的尾气可以通入氨水中,生产氮肥 |
| B.电解精炼时,粗铜应与外电源的正极相连 |
| C.反应2Cu2O+Cu2S→6Cu+SO2↑中的Cu2O是氧化剂 |
| D.每生产6mol Cu,理论上需消耗11mol O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
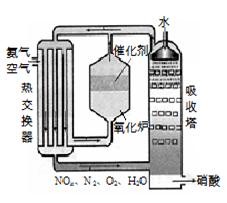
 4NO(g) +6H2O(l) △H<0
4NO(g) +6H2O(l) △H<0 2NO2(g) △H<0
2NO2(g) △H<0 2HNO3(l) +NO(g) △H<0
2HNO3(l) +NO(g) △H<0| A.适当升高温度 |
| B.适当增大吸收塔内的压强 |
| C.增大空气中O2的浓度 |
| D.吸收塔内填充瓷环,增大气液接触面 |
 m3)。假设工业生产硝酸过程中,通过循环操作可以使NH3、O2得以完全利用。
m3)。假设工业生产硝酸过程中,通过循环操作可以使NH3、O2得以完全利用。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.石油的分馏和干馏都是复杂的物理变化和化学变化 |
| B.工业上生产酒精,可以用发酵法和乙烯水化法 |
| C.工业生产聚氯乙烯的反应原理是利用缩聚反应 |
| D.石油裂解气能使溴水褪色,但不能使酸性高锰酸钾褪色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2在食品工业中可以用来防腐、抗氧化、漂白。 |
| B.合成氨工业需要高温高压催化剂 |
| C.硫酸工业中用水吸收SO3 |
| D.硫酸工业中沸腾炉排出的矿渣可供炼铁 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②③ | B.①② | C.①③ | D.①②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com