
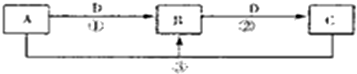
分析 (1)若A可用于自来水消毒,应为Cl2,D是生产、生活中用量最大、用途最广的金属单质,应为Fe,则B为FeCl3,C为FeCl2;
(2)若A是一种碱性气体,常用作制冷剂,应为NH3,B是汽车尾气之一,遇空气会变色,应为NO;
(3)若D是氯碱工业的主要产品,B有两性,由转化关系D为NaOH,B为Al(OH)3,C为NaAlO2;
(4)若A、C、D都是常见气体,C是形成酸雨的主要气体,应为SO2,则A为H2S,D为O2,B为S.
解答 解:(1)若A可用于自来水消毒,应为Cl2,D是生产、生活中用量最大、用途最广的金属单质,应为Fe,则B为FeCl3,C为FeCl2,
工业上制取A的离子方程式为2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH-,故答案为:FeCl3;2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH-;
(2)若A是一种碱性气体,常用作制冷剂,应为NH3,B是汽车尾气之一,遇空气会变色,应为NO,反应①的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(3)若D是氯碱工业的主要产品,B有两性,由转化关系D为NaOH,B为Al(OH)3,C为NaAlO2,反应②的离子方程式是Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)若A、C、D都是常见气体,C是形成酸雨的主要气体,应为SO2,则A为H2S,D为O2,B为S,反应③的化学方程式是2H2S+SO2=3S↓+2H2O,
故答案为:2H2S+SO2=3S↓+2H2O.
点评 本题考查较为综合,涉及元素化合物的推断,为高频考点,侧重于学生的分析能力,物质性质是解题关键,题目具有一定难度,做题时注意把握推断的思路.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L SO3含有NA个分子 | |
| B. | 过氧化钠与CO2反应时,0.1mol过氧化钠转移的电子数为0.2 NA | |
| C. | 6.4 g氧气和3.2 g臭氧(O3)混合气体所含有的氧原子数为0.6 NA | |
| D. | 标准状况下,2.24 L Cl2与过量的稀FeCl2溶液反应,转移电子总数为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 加入试剂 | 稀硫酸 | 浓硫酸、加热 | 稀硝酸 | 浓硝酸 |
| 实验现象 | 红色固体和蓝色溶液 | 无色气体和蓝色溶液 | 无色气体和蓝色溶液 | 红棕色气体和蓝色溶液 |
| A. | Cu | B. | Cu2O | ||
| C. | 一定有Cu,可能有Cu2O | D. | 一定有Cu2O,可能有Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素位于第2周期 | |
| B. | 该元素位于第VI A族 | |
| C. | 该元素的氢化物溶于水显碱性 | |
| D. | 该元素最高价氧化物的水化物是一种弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
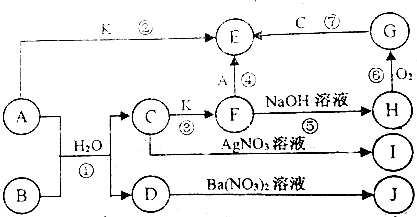
| 实验步骤 | 实验现象 | 用化学用语解释 |
| 将少量气体通入淀粉KI溶液 | 溶液最初变成 蓝 | Cl2+2I-=I2+2Cl- |
| 继续通入气体 | 溶液逐渐变成无色 | 5Cl2+I2+6H2O=2HIO3+10HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C4H8O2的酯有4种结构 | |
| B. | 淀粉和纤维素互为同分异构体 | |
| C. | 乙醇和葡萄糖均能发生酯化反应 | |
| D. | 用氢氧化钠溶液可以鉴别地沟油和矿物油 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
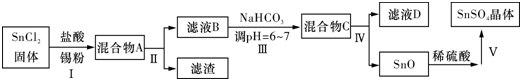
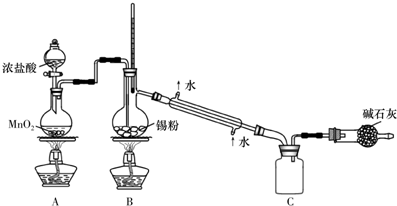
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com