
【题目】硫酸亚铁铵受热分解的反应方程式为![]()
![]()
![]() ,用
,用![]() 表示阿伏加德罗常数的值。下列说法不正确的是 ( )
表示阿伏加德罗常数的值。下列说法不正确的是 ( )
A. 1 L 0.1 mol·L1![]() 溶液中Fe2+的数目小于0.1
溶液中Fe2+的数目小于0.1![]()
B. 将1 mol ![]() 和1 mol
和1 mol ![]() 充分反应后,其分子总数为1.5
充分反应后,其分子总数为1.5![]()
C. 标准状况下,每生成15.68 L气体转移电子数目为0.8![]()
D. 常温常压下,3.0 g![]() 中含有的中子总数为1.6
中含有的中子总数为1.6![]()
【答案】B
【解析】
A.由于Fe2+水解,1L0.1mol·L1(NH4)2Fe(SO4)2溶液中Fe2+的数目小于0.1NA,故A正确;
B.SO2与O2反应2SO2+O2![]() 2SO3属于可逆反应,不能反应完全,若1molSO2和1molO2完全反应生成1molSO3和剩余的0.5molO2,共1.5mol,现不能完全反应,其物质的量大于1.5mol,分子总数大于1.5NA,故B错误;
2SO3属于可逆反应,不能反应完全,若1molSO2和1molO2完全反应生成1molSO3和剩余的0.5molO2,共1.5mol,现不能完全反应,其物质的量大于1.5mol,分子总数大于1.5NA,故B错误;
C.标准状况下,15.68L气体的物质的量为0.7mol,其中NH3占![]() ,N2占
,N2占![]() ,SO2占
,SO2占![]() ,根据反应可知,生成4molSO2转移8mol电子,所以生成0.4molSO2转移0.8mol电子,数目为0.8NA,故C正确;
,根据反应可知,生成4molSO2转移8mol电子,所以生成0.4molSO2转移0.8mol电子,数目为0.8NA,故C正确;
D.15N的中子数=15-7=8,3.0g15N2的物质的量为0.1mol,含有的中子总数为=0.1×16×NA=1.6NA,故D正确。
故选B。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】FeCl2是一种常用的还原剂,有关数据如下:
C6H5Cl(氯苯) | C6H4Cl2 | FeCl3 | FeCl2 | |
溶解性 | 不溶于水,易溶于苯 | 不溶于C6H5Cl,C6H4Cl2,苯,易吸水 | ||
熔点/℃ | -45 | 53 | — | — |
沸点/℃ | 132 | 173 | — | — |
实验室可以用多种方法来制备无水FeCl2。回答下列问题:
Ⅰ.按下如图装置用H2还原无水FeCl3制取。
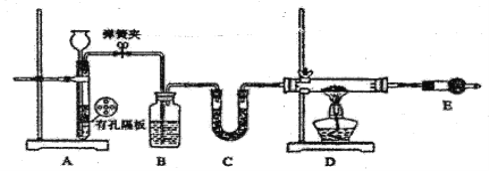
(1)用装置A制取H2,其优点是________________;D中反应的化学方程式为____________________;装置E的作用是____________________________。
(2)通入足量H2,充分反应,如果温度控制不当,产品中会含单质铁,检验产品中是否含铁的方案是____________________________。
Ⅱ.按图装置,在三颈烧瓶中放入162.5g无水氯化铁和225g氯苯,控制反应温度在128℃~139℃加热3h,反应接近100%。反应如下:2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl
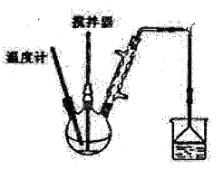
(3)上述反应中,还原剂是____________。
(4)反应温度接近或超过C6H5Cl的沸点,但实验过程中C6H5Cl并不会大量损失,原因是____________________________。
(5)冷却后,将三颈瓶内物质经过过滤,洗涤,干燥后,得到粗产品。
①洗涤所用的试剂可以是____________________________;
②简述回收滤液中C6H5Cl的方案____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列一句话中叙述了两个值,前者记为![]() ,后者记为
,后者记为![]() ,
,![]() 和
和![]() 的关系从A、B、C、D中选择,并填空。
的关系从A、B、C、D中选择,并填空。
A.![]() B.
B.![]() C.
C.![]() D.无法比较
D.无法比较
(1)常温下![]() 的
的![]() 与
与![]()
![]() 等体积混合后溶液中
等体积混合后溶液中![]() 和
和![]() :______;
:______;
(2)同温度下,![]()
![]() 溶液中
溶液中![]() 水解百分率与
水解百分率与![]() 溶液中
溶液中![]() 的水解百分率:______;
的水解百分率:______;
(3)pH值相同的醋酸和盐酸,分别用蒸馏水稀释至原来的![]() 倍和
倍和![]() 倍,稀释后两溶液的
倍,稀释后两溶液的![]() 值仍然相同,则
值仍然相同,则![]() 和
和![]() 的关系是:______;
的关系是:______;
(4)常温下两份等浓度的纯碱溶液,将第二份升高温度,两溶液中![]() :______;
:______;
(5)相同温度下,![]() 值为12的烧碱溶液中水的电离度和
值为12的烧碱溶液中水的电离度和![]() 值为12的
值为12的![]() 溶液中水的电离度:______;
溶液中水的电离度:______;
(6)将![]() 值为2的盐酸和醋酸都稀释相同倍数所得稀溶液的
值为2的盐酸和醋酸都稀释相同倍数所得稀溶液的![]() 值:______;
值:______;
(7)室温下某强酸和某强碱溶液等体积混合后,溶液的![]() 值为7,原酸溶液和原碱溶液的物质的量浓度:______;
值为7,原酸溶液和原碱溶液的物质的量浓度:______;
(8)相同温度下,![]() 的
的![]() 溶液中的
溶液中的![]() 个数和
个数和![]()
![]() 溶液中
溶液中![]() 的个数:______。
的个数:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】发展“碳一化学”,开发利用我国丰富的煤炭资源具有重要的战略意义和经济价值。请回答下列问题:
(1)已知:常温下C(s)的燃烧热△H=-393.5 kJ·mol-1, S(s)的燃娆热△H=-296.0 kJ·mol-l ,CO2(g)+C(S)=2CO(g) △H=+172.5 kJ·mol-1,写出一氧化碳将二氧化硫还原为单质硫的热化学方程式:______
(2)在763 K、3.04×104 kPa时,用CO和H2做原料合成甲醇(CH3OH),存在下列平衡:CO(g)+2H2(g) ![]() CH3OH(g)。当原料中CO和H2的比例不同时,对CO的转化率及平衡混合物中甲醇的体积分数都有影响。
CH3OH(g)。当原料中CO和H2的比例不同时,对CO的转化率及平衡混合物中甲醇的体积分数都有影响。
①设H2和CO起始物质的量之比为m,平衡时CO的转化率为α,平衡混合物中甲醇的体积分数为y,则m、α、y三者的关系式为y=___。
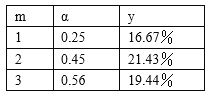
②根据表中提供的数据,可得出反应物的比例对CO的平衡转化率以及平衡混合物中甲醇的体积分数影响的结论,选择最佳反应物配比m=_______(填“l”、“2”或“3”),理由是_________。
(3)如图是四种金属氧化物被一氧化碳还原,反应达到平衡时lgc(CO)/c(CO2)与温度(T)的关系曲线图:

①8000C时,其中最易被还原的金属氧化物是______(填化学式),该反应的平衡常数K=_______。
②CO2还原PbO2的反应△H ___0(填“>”或“<”)。判断依据是_________。
(4)科学家正在研究用固态物质作为火箭推进剂。固体推进剂(硝酸钾和蔗糖的混合物)点燃后在燃烧室里燃烧,发生反应KNO3+C12H22O11→CO2↑+N2↑+H2O+K2CO3,(未配平)。则该反应中氧化剂与还原剂的物质的量之比是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是金属镁和卤素单质(X2)反应的能量变化示意图.下列说法正确的是( )
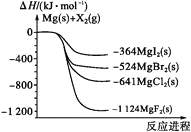
A. 由MgCl2制取Mg是放热过程
B. 热稳定性:MgI2>MgBr2>MgCl2>MgF2
C. 常温下氧化性:F2<Cl2<Br2<I2
D. 由图可知此温度下MgBr2(s)与Cl2(g)反应的热化学方程式为:MgBr2(s) + Cl2(g) ═ MgCl2(s) + Br2(g) △H = -117kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在浓度都为1 mol·L-1的(NH4)2SO4、NH4H CO3、NH4HSO4、NH4Cl的四种溶液中,测得c(NH4+)分别为a、b、c、d(单位为mol·L-1)。下列判断正确的是
A. a=2b=2c=2d B. a>b>c> d C. a>c>d>b D. a>c>b>d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化情况如图所示.则下列说法中不正确的是

A.还原性:I->Fe2+>Br-
B.原混合溶液中FeBr2的物质的量为3mol
C.线段AB表示Fe2+被氯气氧化
D.原溶液中:n(Fe2+):n(I-):n(Br-)═2:1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下各种说法:
①金属和非金属化合时一定形成离子键;
②离子键是阳离子、阴离子的相互吸引力;
③根据电离方程式HCl![]() H++Cl-,判断氯化氢分子里存在离子键;
H++Cl-,判断氯化氢分子里存在离子键;
④氢气和氯气的反应过程:H2、Cl2分子里共价键发生断裂生成H原子、Cl原子,而后H原子、Cl原子形成离子键的过程
上述各种说法正确的是
A. ①② B. 都不正确 C. ①②④ D. ①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.铜粉加入氯化铁溶液中:Cu + Fe3+ = Fe2++Cu2+
B.将稀硫酸滴在铜片上:Cu + 2H+ =Cu2++ H2↑
C.氯气与烧碱溶液反应:Cl2+2OH-=ClO-+Cl-+H2O
D.将少量铜屑放入稀硝酸中:Cu+4H++2NO![]() = Cu2++2NO2↑+2H2O
= Cu2++2NO2↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com