
【题目】下列有关叙述正确的是
A. XX化妆品从纯天然植物中提取,不含任何化学物质
B. 红宝石、玛瑙、水晶、钻石等制作装饰品的材枓,其物质的主要成份都是硅酸盐
C. 氢氧燃料电池、硅太阳能电池中都利用了原电池原理
D. 镧镍合金能大量吸收H2形成金属氢化物,可作储氢材科
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,其中B、D属于常见金属,J是一种黑色固体,I的浓溶液具有还原性,A~I均为中学化学常见物质,它们之间的转化关系如图所示.(部分生成物和反应条件已略去)
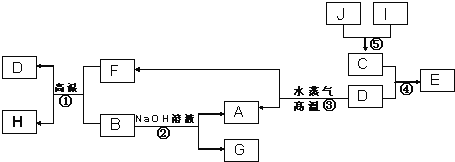
请回答下列问题:
(1)写出组成物质D的元素在周期表中的位置:_________________。
(2)写出反应②的化学方程式:___________________。
(3) J在H2O2分解反应中作催化剂.若将适量J加入酸化的H2O2溶液中,J溶解生成它的+2价离子,该反应的离子方程式是___________________。
Ⅱ.某无色溶液,其中可能存在以下离子:Na+、Ag+、Ba2+、Al3+、AlO2-、S2-、CO32-、SO32-、SO42-,现取该溶液进行有关试验,其结果如下:
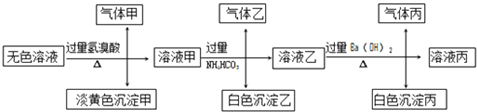
回答下列问题:
(4)生成沉淀甲的离子方程式:__________________;
(5)已知气体甲由两种氧化物组成(不包括水蒸汽和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入下表中(可不填满,表中每一行对应正确方可得分)
步骤 | 实验目的 | 试剂 | 现象 |
1 | |||
2 | |||
3 | |||
4 |
(6)针对溶液中可能存在的离子,用实验验证其是否存在的方法是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的来源、结构与性质说法正确的是
A. 甲烷是正四面体结构,性质活泼,常温下能与强酸、强碱发生剧烈反应
B. 乙烯是通过石油裂解得到的,属于不饱和烃
C. 苯与氢气、液溴、浓硝酸的反应类型相同
D. 乙酸又名醋酸,其官能团是醚基,可以与乙醇发生反应生成乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,氧化剂与还原剂物质的量之比为1:2的是( )
A.3S+6NaOH=2Na2S+Na2SO3+3H2O
B.2CH3COOH+Ca(ClO)2=2HC1O+Ca(CH3COO)2
C.I2+2NaClO=2NaIO3+C12
D.4HCl(浓)+MnO2![]() MnCl2+Cl2+2H2O
MnCl2+Cl2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应:mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为________反应(填“吸热”或“放热”),且m+n________p(填“>”、“=”或“<”)。
(2)减压使容器体积增大时,A的质量分数__________。(填“增大”、“减小”或“不变”,下同)
(3)若加入B(维持体积不变),则A的转化率____________。
(4)若升高温度,则平衡时B、C的浓度之比将____________。
(5)若加入催化剂,平衡时气体混合物的总物质的量__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去)。请填空:
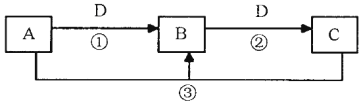
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,则反应②的离子方程式为 ;实验室保存C的水溶液应加入 (填试剂名称)。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为 。
(3)若C是一种能形成硫酸型酸雨的污染性气体,D是一种能支持燃烧和呼吸的气体,则反应③中氧化产物和还原产物的质量比为 。
(4)若D是一种常见的温室气体,A、B、C的的焰色反应都呈黄色,则反应③的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
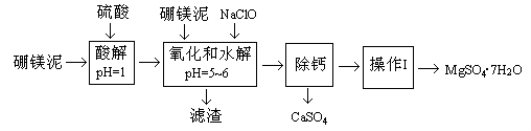
根据题意回答下列问题:
(1)实验中需用1mol/L的硫酸80mL,若用98%的浓硫酸来配制,除量筒、玻璃棒外,还需要的玻璃仪器有 。
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有 。
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式 。
在调节pH=5-6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为 。
(4)如何检验滤液中Fe3+是否被除尽,简述检验方法 。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~J是中学化学中常见的化学物质,它们之间的相互转化关系如下列框图所示(部分反应的产物未列出)。
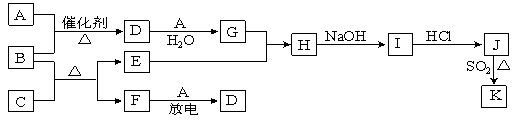
已知:A、F为无色气体单质,B为无色具有刺激性气味的碱性气体,C为黑色氧化物,E为红色金属单质。请回答下列问题:
(1)D的化学式为 ;F的电子式为 。
(2)B和C反应的化学方程式为 。该反应中生成1molF时,转移的电子数为 mol
(3)E与G的稀溶液反应的离子方程式为: 。
(4)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的叙述正确的是
A. 聚乙烯塑料的老化是由于发生了加成反应
B. 苯中含有碳碳双键,其性质跟乙烯相似
C. 乙烯使溴水褪色和苯与溴水混合振荡后水层变为无色原理相同
D. (NH4)2SO4浓溶液和CuSO4溶液都能使蛋白质析出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com