
 ��
�� ��
�� | 1g |
| 16g/mol |
| 1 |
| 16 |
| 55.6kJ/mol | ||
|


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
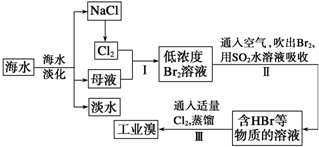
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����
�����
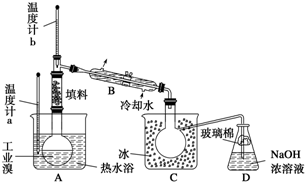
 ��b��
��b�� ��c��H2O2��d��
��c��H2O2��d�� ��e��
��e��
 ��g��O3 ��h��
��g��O3 ��h��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������������ԭ��ͨ��sp3�ӻ�����ɼ�ʱ���÷��Ӳ�һ��Ϊ��������ṹ |
| B�����嵥���У���ϡ�����壩��һ���ЦҼ��������Цм� |
| C���ӻ�ǰ��Ĺ�������䣬���������״�����˸ı� |
| D��sp3��sp2��sp�ӻ�����ļнǷֱ�һ��Ϊ109��28�䡢120�㡢180�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ȵμ���ˮ���ٵμ�KSCN��Һ���Ժ� |
| B��ֻ��μ�KSCN��Һ |
| C���ȵμ�KSCN��Һ�����Ժ�ɫ���ٵμ���ˮ���Ժ�ɫ |
| D����Na2O2�����۲������ɫ�ı仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����������������������ֱ���ȫȼ�գ����߷ų��������� |
| B��������ȼ����Ϊ285.8 kJ/mol��������ȼ�յ��Ȼ�ѧ����ʽΪ��2H2��g��+O2��g��=2H2O��l����H=-285.8 kJ/mol |
| C���ⶨ�к��ȵ�ʵ���У�NaOHҪ�Թ�������ʹHCl��ȫ�к� |
| D��Ba��OH��2?8H2O��s��+2NH4Cl��s��=BaCl2��s��+2NH3��g��+10H2O��l����H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���κ���ʹ��ֵ����Ĺ��̶����Է����� |
| B����֪�Ȼ�ѧ����ʽ2SO2��g��+O2��g��?2SO3��g����H=-Q kJ?mol-1��Q��0������2 mol SO2��g����1 mol O2��g������һ�ܱ������г�ַ�Ӧ��ų�Q kJ������ |
| C����ѧƽ�ⷢ���ƶ���ƽ�ⳣ��һ�������仯 |
| D��1 mol NaOH�ֱ��1 mol CH3COOH��1 mol HNO3��Ӧ�����߱�ǰ�߷ų��������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com