
| A. | 苯中的少量苯酚可先加适量的溴水,再过滤而除去 | |
| B. | 将苯酚晶体放人少量水中,加热时全部溶解,冷却后形成乳浊液 | |
| C. | 苯酚的酸性很弱,不能使酸碱指示剂变色 | |
| D. | 苯酚有毒,但其稀溶液可直接用作防腐剂和消毒剂 |
分析 A.溴易溶于苯,不能除杂,应加NaOH溶液反应后分液来除杂;
B.苯酚为有机物,常温下,苯酚在水中的溶解度不大,当温度高于65℃时,能跟水以任意比例互溶;
C.苯酚的酸性比碳酸弱;
D.苯酚是一种有毒的物质,苯酚的稀水溶液可直接用作防腐剂和消毒剂.
解答 解:A.溴易溶于苯,用溴水除杂,苯酚和溴水反应生成三溴苯酚,三溴苯酚是有机物,溶于苯中,同时会引入新的杂质,则除去苯中的少量苯酚,应向混合物中加入NaOH溶液后分液,故A错误;
B.将苯酚晶体放入少量水中,加热时全部溶解,冷却到50℃形成乳浊液而变浑浊,故B正确;
C.苯酚的酸性很弱,酸性比碳酸还弱,不能使指示剂变色,故C正确;
D.苯酚是一种有毒的物质,能使蛋白质变性,其稀溶液可直接用作防腐剂和消毒剂,故D正确;
故选A.
点评 本题考查了苯酚的性质和用途,题目难度不大,注意把握有机物的性质和用途,注意苯酚的酸性比碳酸弱.


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24L苯中含C-C数目为0.3NA | |
| B. | 常温下9.2gNO2和N2O4的混合气体中含有的氧原子数目为0.4NA | |
| C. | 常温下,1.0LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | |
| D. | 在反应KCO2+6HCl═KCl+3Cl2↑+3H2O中能生成转移电子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a-3}{12}$mol | B. | $\frac{a-27}{12}$mol | C. | $\frac{a-81}{18}$mol | D. | $\frac{a-9}{18}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
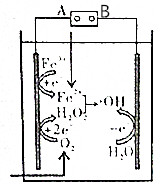 电-Fenton法是用于水体里有机污染物降解的高级氧化技术,其反应原理如图所示,其中电解产生的H2O2与Fe2+发生Fenton反应:Fe2++H2O2=Fe3++OH-+•OH,生成的烃基自由基(•OH)能氧化降解有机污染物.下列说法不正确的是( )
电-Fenton法是用于水体里有机污染物降解的高级氧化技术,其反应原理如图所示,其中电解产生的H2O2与Fe2+发生Fenton反应:Fe2++H2O2=Fe3++OH-+•OH,生成的烃基自由基(•OH)能氧化降解有机污染物.下列说法不正确的是( )| A. | 电源的A极是负极 | |
| B. | 电解池中只有O2、Fe3+发生还原反应 | |
| C. | 阳极上发生电极反应:H2O-e-=•OH+H+, | |
| D. | 消耗1molO2,可以产生4mol•OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在已知元素中具有最大的原子半径 | B. | 在空气中燃烧时生成氧化物Fr2O | ||
| C. | 氧化物对应的水化物是弱碱 | D. | 其单质的熔点比金属钠的熔点高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
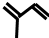 .请回答下列问题:
.请回答下列问题: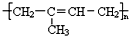 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以上反应均可发生 | B. | 只有⑦不能发生 | ||
| C. | 只有⑥不能发生 | D. | 只有②不能发生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com