
| A. |  火法炼铜 | B. |  中和滴定 | C. |  酿酒 | D. |  制眼镜 |
科目:高中化学 来源: 题型:选择题

| A. | 甲中a的电极反应为:4OH--4e-=O2↑+2H2O | |
| B. | 电解时向乙中滴入酚酞试剂,c电极附近先变红 | |
| C. | 当d电极产生2g气体时,b极有32g物质析出 | |
| D. | 电解少量时间后向乙中加适量盐酸,溶液组成可以恢复到原电解前的状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②⑥ | C. | ③④⑤ | D. | ④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 图甲表示温度T1>T2,SO2与O2反应过程中的能量变化 | |
| B. | 图乙表示0.100 0 mol/L NaOH溶液滴定20.00 mL 0.100 0 mol/L CH3COOH溶液所得到的滴定曲线 | |
| C. | 图丙表示恒容密闭容器中反应“2SO2(g)+O2(g)?2SO3(g)△H<0”的平衡常数K正、K逆随温度的变化 | |
| D. | 图丁表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则aHCl表示溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 分子式为C16H16O7 | |
| B. | 能与钠、乙醇、乙酸、溴发生反应,不能与碳酸钠发生反应 | |
| C. | 能发生取代反应、氧化反应、加成反应,不能发生水解发应 | |
| D. | 1mol 该有机物最多能与2mol NaOH或4mol H2发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | M连接电源正极,N连接电源负极,当两极产生气体总量为22.4mL(标准状况)时,则生成0.001molNaOH | |
| B. | 去掉电源,将M、N用导线直接相连,在溶液中滴入酚酞试液,C电极周围溶液变红 | |
| C. | M连接电源负极,N连接电源正极,如果把烧杯中的溶液换成1LCuSO4溶液,反应一段时间后,烧杯中产生蓝色沉淀 | |
| D. | M连接电源正极,N连接电源负极,将C电极换成Cu电极,电解质溶液换成硫酸铜溶液,则可实现在铁上镀铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
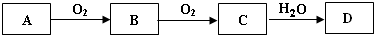
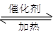 2SO3.
2SO3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
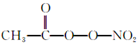 (PAN)等二次污染物.
(PAN)等二次污染物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com