
(14分)I.实验室用Na2CO3·10H2O晶体配制50 g 质量分数为21.2%的Na2CO3溶液。回答下列问题:
(1)应用托盘天平称取Na2CO3·10H2O晶体 g。
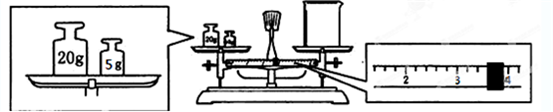
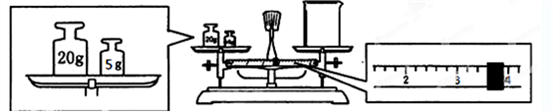
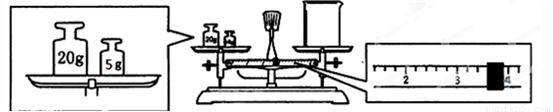
(2)用托盘天平和小烧杯称出碳酸钠晶体的质量,天平平衡后的状态如下图。由图中可以看出,该同学在操作时犯了一个错误是 。实际称量的碳酸钠晶体质量为 g。

II. 实验室要配制2.5 mol/L 的稀硫酸溶液90 mL,回答下列问题:
(1)用量筒量取质量分数为98%,密度为1.84 g/cm3的浓硫酸 mL。
(2)配制时,必须使用的仪器除量筒、烧杯、玻璃棒外,还缺少的仪器是 。
(3)配制溶液的过程中,其他操作都正确,下列操作会使所配溶液浓度偏高的是 。
A.量取浓硫酸时,仰视读数
B.洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
C.稀释硫酸时,有溶液溅到桌面上
D.没有洗涤稀释硫酸的烧杯和玻璃棒
E.定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
F.容量瓶不干燥
(4)从容量瓶中取该溶液40 mL,与5 mol/L的NaOH溶液 mL恰好完全反应,反应后溶液中的c(Na+)= (忽略溶液混合过程中的体积变化)
I.(1)28.6(2分)
(2)砝码和物品的位置放反了(1分) 21.4(1分)
II.(1)13.6(2分)
(2)100 mL容量瓶、胶头滴管(2分)
(3)A B(2分)
(4)40 mL(2分) 2.5 mol/L(2分)
【解析】考查一定物质的量浓度溶液的配制及误差分析等。
I.(1)50 g 质量分数为21.2%的Na2CO3溶液中溶质的质量是50g×21.2%=10.6g,则碳酸钠的物质的量是0.1mol,所以需要Na2CO3·10H2O晶体的质量是0.1mol×286g/mol=28.6g。
(2)根据图示控制,错误是砝码和物品的位置放反了,因此实际固体的质量应该是25-3.6g=21.4g。
II.(1)由于容量瓶的规格没有90ml的,所以应该配制100ml,则需要浓硫酸的体积是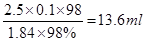 。
。
(2)配制100ml溶液,则一定需要100 mL容量瓶,以及定容时的胶头滴管。
(3)根据c=n/V可知,量取浓硫酸时,仰视读数,则浓硫酸的体积偏大,结果偏高;洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中,则溶质增加,浓度偏高;稀释硫酸时,有溶液溅到桌面上,则溶质减少,浓度偏小;没有洗涤稀释硫酸的烧杯和玻璃棒,则溶质减少,浓度偏小;定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线,则容量瓶中溶液体积增加,浓度偏小;容量瓶不干燥,不会影响实验结果,答案选AB。
(4)40ml溶液中溶质硫酸的物质的量是0.04L×2.5mol/L=0.1mol,所以能消耗0.2mol氢氧化钠,因此需要氢氧化钠溶液的体积是40ml。反应后钠离子的浓度是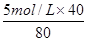 =2.5
mol/L。
=2.5
mol/L。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012-2013学年重庆市重庆一中高一10月月考化学试卷(带解析) 题型:实验题
(14分)I.实验室用Na2CO3·10H2O晶体配制50 g质量分数为21.2%的Na2CO3溶液。回答下列问题:
(1)应用托盘天平称取Na2CO3·10H2O晶体 g。
(2)用托盘天平和小烧杯称出碳酸钠晶体的质量,天平平衡后的状态如下图。由图中可以看出,该同学在操作时犯了一个错误是 。实际称量的碳酸钠晶体质量为 g。
II. 实验室要配制2.5 mol/L 的稀硫酸溶液90 mL,回答下列问题:
(1)用量筒量取质量分数为98%,密度为1.84 g/cm3的浓硫酸 mL。
(2)配制时,必须使用的仪器除量筒、烧杯、玻璃棒外,还缺少的仪器是 。
(3)配制溶液的过程中,其他操作都正确,下列操作会使所配溶液浓度偏高的是 。
| A.量取浓硫酸时,仰视读数 |
| B.洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中 |
| C.稀释硫酸时,有溶液溅到桌面上 |
| D.没有洗涤稀释硫酸的烧杯和玻璃棒 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:2012-2013学年天津一中高一(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com