
 �������������ڹ�ҵ�϶�����Ҫ����;����֪��������ϡ���ᷴӦ�����������������Ǹ���CrSO4����ͭ������ԭ�����ͼ��ʾ��������װ���DZ���KCl��֬��Һ�����й��ڴ˵�ص�˵����ȷ���ǣ�������
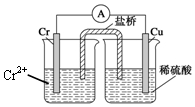
�������������ڹ�ҵ�϶�����Ҫ����;����֪��������ϡ���ᷴӦ�����������������Ǹ���CrSO4����ͭ������ԭ�����ͼ��ʾ��������װ���DZ���KCl��֬��Һ�����й��ڴ˵�ص�˵����ȷ���ǣ�������| A�� | ���ŵ�������ʹ����װ�ù���ͨ·��������Һ�ʵ����ԣ����������ŵ�ԭ��أ������о������ñ���KCl��֬��Һ | |
| B�� | ������1molCr�ܽ⣬�����н���2molCl-������أ�2molK+�����ҳ� | |
| C�� | �˹�����H+�õ��ӣ�����������Ӧ | |
| D�� | ���ӴӸ���ͨ�����ߵ�ͭ������ͨ�����ŵ�ת�Ƶ����ձ��� |
���� A�������в��Ƕ������ñ���KCl��֬��Һ��Ҫ�����ܷ���������Һ��Ӧ��
B.1molCr��Ӧ��ת��2mol���ӣ�
C�������ӵõ��ӷ�����ԭ��Ӧ��
D���������������ƶ�������ͨ����
��� �⣺A�������в��Ƕ������ñ���KCl��֬��Һ�����������ҺΪ��������Һʱ�������ɳ�������A����
B.1molCr��Ӧ��ת��2mol���ӣ�Ϊ���ֵ���غ㣬�����н���2molCl-������أ�2molK+�����ҳأ���B��ȷ��
C�������ӵõ��ӷ�����ԭ��Ӧ����C����
D���������������ƶ�������ͨ������D����
��ѡB��
���� ���⿼����ԭ��ع���ԭ���Լ����ŵ����ã���Ŀ�ѶȲ���ע�������в�һ�������ñ����Ȼ�����Һ��ѡ��A�״���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
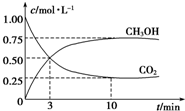 Ϊ̽����CO2������ȼ�ϼ״��ķ�Ӧԭ�����ֽ�������ʵ�飺�����Ϊ1L���ܱ������У�����1mol CO2��3molH2��һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ•mol-1��T�¶��£����CO2��CH3OH��g����Ũ����ʱ��仯��ͼ����ش��������⣺
Ϊ̽����CO2������ȼ�ϼ״��ķ�Ӧԭ�����ֽ�������ʵ�飺�����Ϊ1L���ܱ������У�����1mol CO2��3molH2��һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ•mol-1��T�¶��£����CO2��CH3OH��g����Ũ����ʱ��仯��ͼ����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
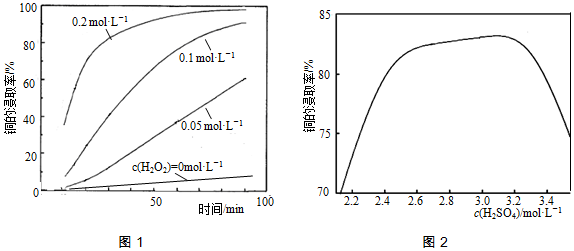
| A�� | �ױ���ʹ����KMnO4��Һ��ɫ�������ͼ��鲻�� | |
| B�� | �����ܸ�NaOH��Һ��Ӧ���Ҵ����� | |
| C�� | ��ϩ�ܷ����ӳɷ�Ӧ�����鲻�� | |
| D�� | ����50-60��ʱ����������Ӧ���������������ױ���30��ʱ���ɷ���������Ӧ�����������ױ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ�Ľṹ��ʽΪCH2CH2 | B�� | �ǻ��ĵ���ʽ��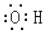 | ||
| C�� | ���ӵĽṹ��ʽΪC6H5OH | D�� | �Ҵ��ķ���ʽ��CH3CH2OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
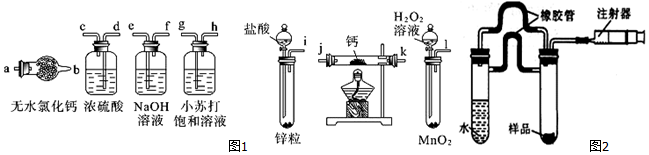
| A�� | 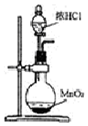 ����ͼװ����ȡ���� | |
| B�� | 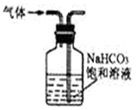 ����ͼװ�ó�ȥCO2�е�����SO2���� | |
| C�� | 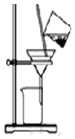 ����ͼװ�÷��뱥��Na2CO3��Һ�е�NaHCO3���� | |
| D�� | 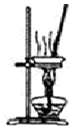 ����ͼװ�ý�MgCl2.6H2O���ȵõ�MgCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ����� | B�� | ����Ⱦ�Ŀ��� | C�� | ��ˮ | D�� | Ư�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com