
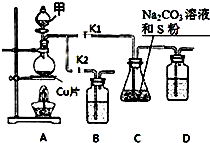
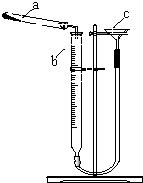
 硫代硫酸钠(Na2S2O3)在工业生产、医药制造业中被广泛应用,工业普遍使用Na2SO3与硫磺(S)共煮得到,装置如图.已知:Na2S2O3在酸性溶液中不能稳定存在.
硫代硫酸钠(Na2S2O3)在工业生产、医药制造业中被广泛应用,工业普遍使用Na2SO3与硫磺(S)共煮得到,装置如图.已知:Na2S2O3在酸性溶液中不能稳定存在.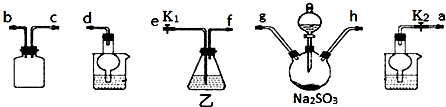
分析 (1)Na2SO3与硫磺(S)共煮可制得硫代硫酸钠,装置C中试剂为Na2CO3溶液和硫粉,所以试剂甲与铜片反应生成SO2,则试剂甲为浓硫酸,铜与浓硫酸反应生成硫酸铜和二氧化硫;
(2)①Na2S2O3在酸性溶液中不能稳定存在、碳酸根与氢离子不大量共存;
②装置B、D中应盛放氢氧化钠溶液,用来吸收SO2,防止污染环境;
(3)三颈烧瓶中是浓硫酸和亚硫酸钠反应生成二氧化硫气体的装置,乙中发生反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2,标有a、d装置进行尾气吸收,防止污染空气,标有bc的装置为安全瓶,起到防止倒吸的作用,反应结束后,先关闭分液漏斗旋塞,接下来的操作是关闭K1打开K2;
(4)装置乙中发生反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2;
(5)Na2S2O3与足量氯水反应,氯气是强氧化剂,硫代硫酸钠中硫元素被氧化为硫酸根,氯元素被还原为C1-;
(6)证明残留的Cl2被还原成了Cl-,先加入硝酸钡除掉硫酸根,取上层液用硝酸银溶液检验氯离子.
解答 解:(1)Na2SO3与硫磺(S)共煮可制得硫代硫酸钠,装置C中试剂为Na2CO3溶液和硫粉,所以试剂甲与铜片反应生成SO2,则试剂甲为浓硫酸,铜与浓硫酸反应生成硫酸铜和二氧化硫,反应方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2SO2↑+2H2O;
(2)①Na2S2O3在酸性溶液中不能稳定存在、碳酸根与氢离子不大量共存,反应离子方程式:S2O32-+2H+=H2O+SO2↑+S↓、CO32-+2H+=H2O+CO2↑、
故答案为:S2O32-+2H+=H2O+SO2↑+S↓、CO32-+2H+=H2O+CO2↑;
②装置B、D中应盛放氢氧化钠溶液,用来吸收SO2,防止污染环境,故答案为:氢氧化钠溶液;
(3)三颈烧瓶中是浓硫酸和亚硫酸钠反应生成二氧化硫气体的装置,乙中发生反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2,标有a、d装置进行尾气吸收,防止污染空气,标有bc的装置为安全瓶,起到防止倒吸的作用,反应结束后,先关闭分液漏斗旋塞,接下来的操作是关闭K1打开K2,接口顺序为:a→g,h→b,c→e,f→d或 a→h,g→b,c→e,f→d,
故答案为:g、h、b、c、e、f或 h、g、b、c、e、f;
(4)装置乙中发生反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2,盛装的试剂是Na2CO3和Na2S的混合溶液,
故答案为:Na2CO3和Na2S的混合溶液;
(5)Na2S2O3与氯气反应生成硫酸根,氯元素被还原为C1-,离子方程式为:S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+,
故答案为:S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+;
(6)证明上述残留的Cl2被还原成了Cl-方法为:取少量反应后的溶液于试管中,滴入Ba(NO3)2溶液至不再产生沉淀,再取上层清液(或过滤后取滤液),滴加AgNO3溶液,若产生白色沉淀,则说明Cl2被还原为了Cl-,
故答案为:取少量反应后的溶液于试管中,滴入Ba(NO3)2溶液至不再产生沉淀,再取上层清液(或过滤后取滤液),滴加AgNO3溶液,若产生白色沉淀,则说明Cl2被还原为了Cl-.
点评 本题考查物质的制备实验,侧重考查学生对制备原理的分析,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和规范严谨的实验设计能力,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | R的氢化物比Y的氢化物的沸点更高 | |
| B. | X与Z组成的化合物溶于水呈碱性 | |
| C. | 只有Y元素存在同素异形体 | |
| D. | X、Y、Z、R形成简单离子的半径依次增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
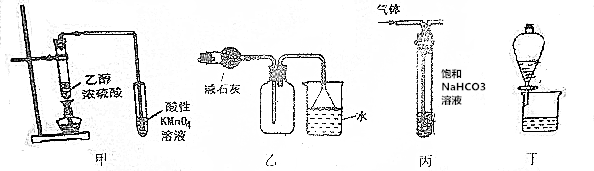
| A. | 装置甲可用于检验乙烯生成 | |
| B. | 装置乙可用于收集和吸收氨气 | |
| C. | 装置丙可用于出去CO2中混有的SO2气体 | |
| D. | 装置丁可分离碘的CCl4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.
碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.| 实验序号 | 样品质量/g | CO2体积/mL(已折算成标准状况下) |
| 1 | 0.542 | 44.82 |
| 2 | 0.542 | 44.80 |
| 3 | 0.542 | 44.78 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| n(CO2)(mol) | 2 | 3 | 4 | 6 |
| n(沉淀)(mol) | 2 | 2 | 3 | 3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠溶液中通入足量二氧化硫:SO2+2OH-═SO32-+H2O | |
| B. | 石灰水与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 钠与水反应:Na+2H2O═2OH-+Na++H2↑ | |
| D. | 向少量碳酸氢钠溶液中滴加足量澄清石灰水:HCO${\;}_{3}^{-}$+Ca2++OH-═CaCO3↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com