
| A、在pH=1的溶液中,Cu2+、Fe2+、NO3-和SO42-能大量共存 |
| B、用惰性电极电解饱和氯化钠溶液的离子方程式:2Cl-+2H+=H2↑+Cl2↑ |
| C、镁铝合金被碱液腐蚀时,负极反应式为:Mg-2e-=Mg2+ |
| D、大量使用含磷洗涤剂会造成水体富营养化 |
| ||


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案科目:高中化学 来源: 题型:
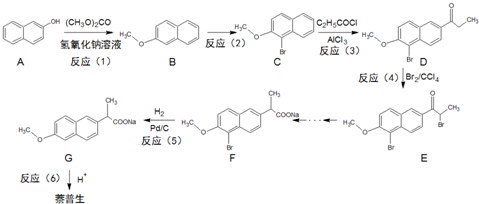
 )的化学性质与苯相似.
)的化学性质与苯相似.| 反应试剂 |
| 反应条件 |
| 反应试剂 |
| 反应条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
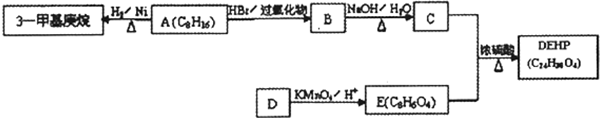
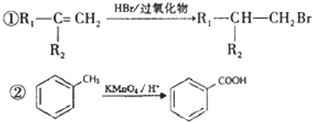
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、牙膏中甘油是保湿剂和甜味剂,可用新制氢氧化铜检验 |
| B、滴定实验中所用到的滴定管、移液管,在使用前均需干燥或用相应的溶液润洗,容量瓶、锥形瓶则不应润洗 |
| C、火柴头中的氯元素检验的实验中,将火柴头(未燃烧)浸于水中,片刻后取少量溶液,加AgNO3溶液、稀硝酸,若出现白色沉淀,证明有氯元素 |
| D、培养明矾晶体时,为得到较大颗粒的晶体,应自然冷却,并静置过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、往CrCl3溶液加入过量NaOH溶液可制得Cr(OH)3 |
| B、对CrCl3?6H2O加热脱水可得CrCl3 |
| C、Cr2O3既能溶于酸,又能溶于NaOH溶液 |
| D、[Cr(OH)4]-水溶液显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
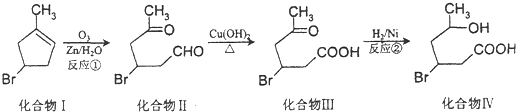
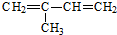 (2-甲基-1,3-丁二烯)发生类似①的反应,得到有机物Ⅵ和Ⅶ,结构简式分别是为
(2-甲基-1,3-丁二烯)发生类似①的反应,得到有机物Ⅵ和Ⅶ,结构简式分别是为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com