
| A�� | ��ѧ�ҿ������۲����ϲ��ݷ��Ӻ�ԭ�ӣ���װ���Ӳ��� | |
| B�� | ��ѧ��һ�ž��д����ԵĿ�ѧ����ѧ������������ʶ���Ӻ�������� | |
| C�� | ��ѧ����ԭ�ӡ����ӵ�ˮƽ���о����ʵ�һ����Ȼ��ѧ | |
| D�� | ��ѧע�����۷�����������������Ҫ����ѧʵ�� |
���� A����ѧ�ҿ������۲����ϲ��ݷ��Ӻ�ԭ�ӣ���װ���Ӳ��ϡ����������ͷ��ӻ�����
B����ѧ���о�Ŀ���ǰ���������ʶ�������Ӧ�����ʣ�
C����ѧ���о����ʵ���ɡ��ṹ�����ʡ��Լ��仯���ɵĿ�ѧ��
D����ѧ��һ����ʵ��Ϊ�����Ŀ�ѧ����ѧ������Ҫʵ���Ǵ���ģ�
��� �⣺A����ѧ�ķ�չ�dz�Ѹ�٣���ѧ�ҿ������۲����ϲ��ݷ��Ӻ�ԭ�ӣ��Ӷ��÷��ӻ�ԭ������װ���Ӳ��ϡ����������ͷ��ӻ�������A��ȷ��
B����ѧ�о�����ҪĿ���ǣ���ʶ���ʵ���ɡ��ṹ������ԭ�ӡ����ӡ����ӵ������������Լ��仯���ɣ����������Ƚ��ļ������豸������µķ��ӣ���B��ȷ��
C����ѧ���о����ʵ���ɡ��ṹ�����ʡ��Լ��仯���ɣ���;���Ʒ��ȷ����һ����Ȼ��ѧ����C��ȷ��
D����ѧ��һ����ʵ��Ϊ�����Ŀ�ѧ�����л�ѧʵ�飬�۲�ʵ������ͨ�����������ó���ȷ�Ľ����ǻ�ѧѧϰ�ķ���֮һ������Ҫʵ���Ǵ���ģ���D����
��ѡD��
���� ���⿼���˻�ѧ��ѧ�Ķ������������Ŀ�ѶȲ���ע�⻯ѧ��ѧ���ڷ��ӡ�ԭ��ˮƽ���о����ʣ�


 �ظ���ʦ�㲦ϵ�д�
�ظ���ʦ�㲦ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�������Һ��ͨ��������Fe2++Cl2=Fe3++2Cl- | |
| B�� | �ں����ҵĽ���Һ������I-���еμ�H2O2�õ�I2��2I-+H2O2+2H+=I2+O2��+2H2O | |
| C�� | ������Һ��ͨ������CO2��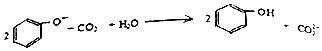 | |
| D�� | ���������Ũ�ȵ�Ba��OH��2ϡ��Һ��NH4HCO3ϡ��Һ��ϣ�Ba2++2OH-+NH4++HCO3-=BaCO3��+NH3•H2O+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪2C��s��+O2��g��=2CO��g����H=-221 kJ•mol-1�����֪C��ȼ����Ϊ-110.5 kJ•mol-1 | |
| B�� | ��101kPa��������ȼ���ȡ�H=-285.8 kJ•mol-1����ˮ�ֽ���Ȼ�ѧ����ʽ��2 H2O ��l��=2H2 ��g��+O2 ��g����H=+285.8 kJ•mol-1 | |
| C�� | Ba��OH��2��aq��+H2SO4��aq��=BaSO4��s��+2H2O��l����H=-2akJ•mol-1�����κ�ǿ���ǿ����кͷ�Ӧ����1molH2O��l���ķ�Ӧ�Ⱦ�Ϊ-akJ•mol-1 | |
| D�� | 1g������ȫȼ������Һ̬ˮ�Ĺ����зų�55.6kJ��������CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-889.6kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 | B�� | 3 | C�� | 2 | D�� | 1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ӦʽΪMg-2e-�TMg2+ | |
| B�� | �������ܻᷢ������ӦMg+2H2O�TMg��OH��2+H2�� | |
| C�� | ��طŵ�ʱCl-�ɸ���������Ǩ�� | |
| D�� | ������ӦʽΪAgCl+e-�TAg+Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
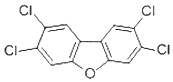 ���ʳ����ʳ�ﰲȫ������ǰ������������բз��ֳ����������������fӢ�����������������꣮2��4��7��8-���ȶ�����������е�һ�֣��ṹ��ʽ��ͼ�������йظ����ʵ�˵����ȷ���ǣ�������
���ʳ����ʳ�ﰲȫ������ǰ������������բз��ֳ����������������fӢ�����������������꣮2��4��7��8-���ȶ�����������е�һ�֣��ṹ��ʽ��ͼ�������йظ����ʵ�˵����ȷ���ǣ�������| A�� | �ܷ���������Ӧ | B�� | һ��ȡ����ֻ��һ�� | ||
| C�� | �����ȴ������� | D�� | ������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
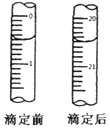 ���ѪҺ�е�Ca2+�ܹ������ж϶��ּ�����ij�о�С��ⶨѪҺ��Ʒ��Ca2+�ĺ�����l00mLѪҺ�к�Ca2+����������ʵ�鲽�����£�
���ѪҺ�е�Ca2+�ܹ������ж϶��ּ�����ij�о�С��ⶨѪҺ��Ʒ��Ca2+�ĺ�����l00mLѪҺ�к�Ca2+����������ʵ�鲽�����£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | H2S | B�� | SO2 | C�� | SO2��O2 | D�� | SO2��H2S |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���Ĵ�ʡ������10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij����˻��ϣ��и����˶�Ա������˷ܼ���ȡ���������ʸ���ͼ�Ǽ����˷ܼ���ij��ͬϵ��X�Ľṹ������X��˵����ȷ���ǣ� ��

A��X�����в���������ԭ�Ӷ���ͬһƽ����
B��X ����FeCl3��Һʱ����ɫ��������ʹ������Ȼ�̼��Һ��ɫ
C��1 mol X ��������Ũ��ˮ��Ӧ���������5 mol Br2
D��1 mol X��һ����������������������Ӧ���������1 mol H2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com