
| A. | 偏二甲肼既是氧化剂又是还原剂 | |
| B. | 该反应进行时只有放热过程没有吸热过程 | |
| C. | 该反应中氮元素的化合价升高 | |
| D. | 该反应中每生成1mol CO2转移8mol电子 |
分析 在反应C2H8N2+2N2O4=2CO2↑+3N2↑+4H2O中,C2H8N2中N元素的化合价为-3价,H为+1价,C为-1价,N2O4中N为+4价,根据化合价的变化解答该题.
解答 解:A.C2H8N2中N元素的化合价为-3价,反应时化合价的变化为:C化合价由-1价升高为+4价,N化合价由-3价升高为0价,则该反应中C2H8N2为还原剂,被氧化,故A错误;
B.反应放热,为火箭升空提供能量,水由液态生成气态为吸热过程,故B错误;
C.该反应的反应物C2H8N2中C化合价由-1价升高为+4价,N化合价由-3价升高为0价,C和N元素的化合价都升高,故C正确;
D.2molN2O4反应得到2×2×(4-0)mol=16mol电子,生成2molCO2,则生成1molCO2,转移8mol电子,故D正确.
故选CD.
点评 本题考查氧化还原反应,为高频考点,注意正确分析各元素化合价的变化为解答该题的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 甲苯苯环上的1个氢原子被含3个碳原子的烷基取代,所得产物有6种 | |
| B. | 已知丙烷的二氯代物有4种异构体,则其六氯代物的异构体数目也为4种 | |
| C. | 含有5个碳原子的某饱和链烃,其一氯代物有3种 | |
| D. | 菲的结构为 ,它与硝酸反应,可生成5种一硝基取代物 ,它与硝酸反应,可生成5种一硝基取代物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
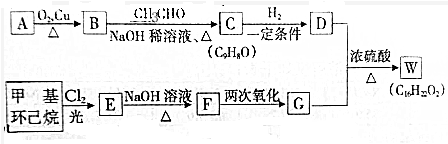
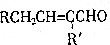 +H2O(R、R′为H或烃基)
+H2O(R、R′为H或烃基)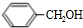 ;C中含有的官能团为碳碳双键、醛基(写名称).
;C中含有的官能团为碳碳双键、醛基(写名称).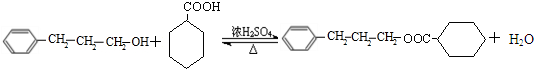 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浊液a中存在沉淀溶解平衡:BaSO4(s)?Ba2+(aq)+SO42-(aq) | |
| B. | 若向滤液b中滴加0.01mol•L-1Na2SO4溶液,无明显现象 | |
| C. | 若向滤液b中滴加0.01mol•L-1BaCl2溶液,会出现白色沉淀 | |
| D. | 若向滤液b中滴加0.01mol•L-1AgNO3溶液,无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水稀释后,溶液中$\frac{c(O{H}^{-})}{c(Cl{O}^{-})}$增大 | |
| B. | 溶液中c(ClO-)>c(HClO)>c(OH-)>c(H+) | |
| C. | 溶液中2c(Ca2+)+c(H+)=c(ClO-)+c(OH-) | |
| D. | 若溶液的pH=l2,则c(ClO-)的水解百分率约为9.1% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应物所具有的总能量等于生成物所具有的总能量 | |
| B. | 最终可生成0.2 mol NH3 | |
| C. | 反应达平衡后,使用催化剂,不能使平衡向右移动 | |
| D. | 当n(N2):n(H2)=1:3时,一定达化学平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制的氯水保存在棕色广口瓶中,并放在阴凉处 | |
| B. | 溴水存放在带玻璃塞的无色试剂瓶中 | |
| C. | 烧碱溶液放在带玻璃塞的磨口试剂瓶中 | |
| D. | 金属钠保存在煤油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.5mol•L-1•mim-1 | B. | v(B)=0.3mol•L-1•mim-1 | ||
| C. | v(C)=0.8mol•L-1•mim-1 | D. | v(D)=0.1mol•L-1•s-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com