
”¾ĢāÄæ”æŌŚŅ»¶ØĢõ¼žĻĀ£¬ĆܱÕČŻĘ÷ÄŚ·¢ÉśæÉÄę·“Ó¦3A+m Bn C“ļµ½Ę½ŗā£®
£Ø1£©ČōA”¢C¾łĪŖĘųĢ壬BĪŖ¹ĢĢ壬ŌņĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK=£»
£Ø2£©ČōA”¢B”¢C¾łĪŖĘųĢ壬ŌŚ¼õŠ”Ń¹ĒæŹ±Ę½ŗāÕżĻņŅĘ¶Æ£¬Ōņ3+mn£ØĢī”°£¾”±”¢”°£¼”±»ņ”°=”±£©£»
£Ø3£©ČōøĆ·“Ó¦ŌŚČĪŗĪĪĀ¶ČĻĀ¶¼ÄÜ×Ō·¢½ųŠŠ£¬Ōņ”÷H£¼0£¬”÷S0£ØĢī”°£¾”±”¢”°£¼”±»ņ”°=”±£©£®
”¾“š°ø”æ
£Ø1£©![]()
£Ø2£©£¼
£Ø3£©£¾
”¾½āĪö”æ½ā£ŗ£Ø1£©Ę½ŗā³£ŹżµČÓŚÉś³ÉĪļÅضČĆŻÖ®»ż±ČÉĻ·“Ó¦ĪļÅضČĆŻÖ®»ż£¬¹ĢĢåĪļÖŹ²»“śČė±ķ“ļŹ½£¬ĖłŅŌK= ![]() £¬ĖłŅŌ“š°øŹĒ£ŗ
£¬ĖłŅŌ“š°øŹĒ£ŗ ![]() £»£Ø2£©A”¢B”¢C¾łĪŖĘųĢ壬ŌŚ¼õŠ”Ń¹ĒæŹ±Ę½ŗāÕżĻņŅĘ¶Æ£¬ĖµĆ÷Õż·“Ó¦·½ĻņŹĒĘųĢåŌö“óµÄ·½Ļņ£¬ĖłŅŌ3+m£¼n£¬ĖłŅŌ“š°øŹĒ£ŗ£¼£»£Ø3£©”÷H£¼0£¬ČōÄܹ»Āś×ć”÷G=”÷H©T”÷S£¼0£¬ģŲÖµŌö“󼓔÷S£¾0£¬ŌŚČĪŗĪĪĀ¶ČĻĀ¶¼ÄÜ×Ō·¢½ųŠŠ£¬ĖłŅŌ“š°øŹĒ£ŗ£¾£®
£»£Ø2£©A”¢B”¢C¾łĪŖĘųĢ壬ŌŚ¼õŠ”Ń¹ĒæŹ±Ę½ŗāÕżĻņŅĘ¶Æ£¬ĖµĆ÷Õż·“Ó¦·½ĻņŹĒĘųĢåŌö“óµÄ·½Ļņ£¬ĖłŅŌ3+m£¼n£¬ĖłŅŌ“š°øŹĒ£ŗ£¼£»£Ø3£©”÷H£¼0£¬ČōÄܹ»Āś×ć”÷G=”÷H©T”÷S£¼0£¬ģŲÖµŌö“󼓔÷S£¾0£¬ŌŚČĪŗĪĪĀ¶ČĻĀ¶¼ÄÜ×Ō·¢½ųŠŠ£¬ĖłŅŌ“š°øŹĒ£ŗ£¾£®
”¾æ¼µć¾«Īö”æ¹ŲÓŚ±¾Ģāæ¼²éµÄ»ÆŃ§Ę½ŗāדĢ¬±¾ÖŹ¼°ĢŲÕ÷£¬ŠčŅŖĮĖ½ā»ÆŃ§Ę½ŗāדĢ¬µÄĢŲÕ÷£ŗ”°µČ”±¼“ VÕż=VÄę>0£»”°¶Æ”±¼“ŹĒ¶ÆĢ¬Ę½ŗā£¬Ę½ŗāŹ±·“Ó¦ČŌŌŚ½ųŠŠ£»”°¶Ø”±¼“·“Ó¦»ģŗĻĪļÖŠø÷×é·Ö°Ł·Öŗ¬Įæ²»±ä£»”°±ä”±¼“Ģõ¼žøÄ±ä£¬Ę½ŗā±»“ņĘĘ£¬²¢ŌŚŠĀµÄĢõ¼žĻĀ½ØĮ¢ŠĀµÄ»ÆŃ§Ę½ŗā£»ÓėĶ¾¾¶ĪŽ¹Ų£¬Ķā½ēĢõ¼ž²»±ä£¬æÉÄę·“Ó¦ĪŽĀŪŹĒ“ÓÕż·“Ó¦æŖŹ¼£¬»¹ŹĒ“ÓÄę·“Ó¦æŖŹ¼£¬¶¼æɽØĮ¢Ķ¬Ņ»Ę½ŗāדĢ¬£ØµČŠ§£©²ÅÄÜµĆ³öÕżČ·“š°ø£®


 ²¹³äĻ°Ģā½ĖÕĻµĮŠ“š°ø
²¹³äĻ°Ģā½ĖÕĻµĮŠ“š°ø ѧĮ·æģ³µµĄæŚĖćŠÄĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
ѧĮ·æģ³µµĄæŚĖćŠÄĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖ«°²Ķ×Ć÷æÉÓĆÓŚ½µµĶŃŖŅŗÖŠµÄµØ¹Ģ“¼£¬Ęä½į¹¹¼ņŹ½ĪŖ£ŗ 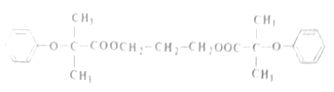
øĆĪļÖŹµÄŗĻ³ÉĻßĀ·ČēĶ¼£ŗ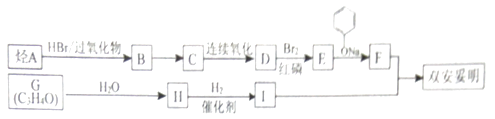
ŅŃÖŖ£ŗI£®RCH2COOH ![]()
![]()
![]()
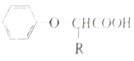
II£®RCHØTCH2 ![]() RCH2CH2Br
RCH2CH2Br
III£®Ķ¬ĪĀĶ¬Ń¹ĻĀAµÄĆܶȏĒH2ĆܶȵÄ28±¶£¬ĒŅÖ§Į“ÓŠŅ»øö¼×»ł£»GÄÜ·¢ÉśŅų¾µ·“Ó¦£¬ĒŅ1molGÄÜÓė2molH2·¢Éś¼Ó³É·“Ó¦£®
£Ø1£©Ė«°²Ķ×Ć÷µÄ·Ö×ÓŹ½ĪŖ £®
£Ø2£©AµÄ½į¹¹¼ņŹ½ĪŖ £®
£Ø3£©·“Ó¦B”śCµÄ·“Ó¦Ģõ¼žŹĒ £¬ G”śHµÄ·“Ó¦ĄąŠĶŹĒ £®
£Ø4£©·“Ó¦”°F+I”śĖ«°²Ķ×Ć÷”±µÄ»Æѧ·½³ĢŹ½ĪŖ £®
£Ø5£©·ūŗĻĻĀĮŠ3øöĢõ¼žµÄFµÄĶ¬·ÖŅģ¹¹ĢåÓŠÖÖ£®Ģõ¼ž£ŗ¢ŁÓėFeCl3ČÜŅŗĻŌÉ«£»¢Ś±½»·ÉĻÖ»ÓŠĮ½øöČ”“ś»ł£»¢Ū1moløĆĪļÖŹ×ī¶ąæÉÓė3molNaOH·“Ó¦£®
£Ø6£©²ĪÕÕÉĻŹöŗĻ³ÉĀ·Ļߣ¬ĒėÉč¼ĘÓÉ ![]() £Ø
£Ø ![]() Óė±½»·ŠŌÖŹĻąĖĘ£©Óė
Óė±½»·ŠŌÖŹĻąĖĘ£©Óė ![]() ŗĻ³É
ŗĻ³É 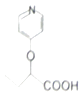 µÄĀ·Ļߣŗ £®
µÄĀ·Ļߣŗ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅÖŠŠčŅŖÅäÖĘ2 mol/LµÄNaOHČÜŅŗ950 mL£¬ÅäÖĘŹ±Ó¦Ń”ÓƵÄČŻĮæĘæµÄ¹ęøńŗĶ³ĘČ”µÄNaOHµÄÖŹĮæ·Ö±šŹĒ(””””)
A. 950 mL””76.0 g B. 500 mL””80.0 g
C. 1 000 mL””80.0 g D. 1 000 mL””76.0 g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ĢÖÜĘŚŌŖĖŲQ”¢R”¢T”¢WŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēÓŅĶ¼ĖłŹ¾£¬ĘäÖŠTĖł“¦µÄÖÜĘŚŠņŹżÓėÖ÷×å×åŠņŹżĻąµČ£¬Ēė»Ų“šĻĀĮŠĪŹĢā
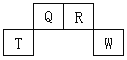
£Ø1£©QŌŖĖŲŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖ________”£
£Ø2£©TŌŖĖŲµÄĄė×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ_____________”£
£Ø3£©ŌŖĖŲµÄ·Ē½šŹōŠŌ(Ō×ӵĵƵē×ÓÄÜĮ¦)£ŗQ_______R£ØĢī”°ĒæÓŚ”±»ņ”°ČõÓŚ”±£©£¬æÉ×÷ĪŖ¶žÕß·Ē½šŹōĒæČõµÄÅŠ¶ĻŅĄ¾ŻŹĒ________________________________________________”£
£Ø4£©WµÄµ„ÖŹÓėĘä×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļÅØČÜŅŗ¹²ČČÄÜ·¢Éś·“Ó¦£¬Éś³ÉĮ½ÖÖĪļÖŹ£¬ĘäÖŠŅ»ÖÖŹĒĘųĢ壬øĆĘųĢåÄÜŹ¹Ę·ŗģČÜŅŗĶĖÉ«£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ____________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»¶ØĪĀ¶ČĻĀ£¬½«2mol AŗĶ2mol BĮ½ÖÖĘųĢå»ģŗĻÓŚ2LĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦3A£Øg£©+B£Øg£©xC£Øg£©+2D£Øg£©£¬2minÄ©·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬Éś³É0.8mol D£¬²¢²āµĆCµÄÅضČĪŖ0.4mol/L£®ÓÉ“ĖĶʶĻ£ŗ
£Ø1£©xÖµµČÓŚ£»
£Ø2£©AµÄ×Ŗ»ÆĀŹĪŖ£»
£Ø3£©BµÄĘ½ŗāÅضČĪŖmol/L£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪĀ¶ČŹ±£¬Ā±»ÆŅų£ØAgX£¬X=Cl£¬Br£¬I£©µÄ3ĢõČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£¬AgCl”¢AgBr”¢AgIµÄKspŅĄ“Ī¼õŠ”£®ŅŃÖŖpAg=©lgc£ØAg+£©£¬pX=©lgc£ØX©£©£¬ĄūÓĆpX”¢pAgµÄ×ų±źĻµæɱķŹ¾³öAgXµÄČܶȻżÓėČÜŅŗÖŠµÄc£ØAg+£©ŗĶc£ØX©£©µÄĻą»„¹ŲĻµ£®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø £© 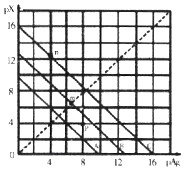
A.AĻߏĒAgClµÄČܽāĘ½ŗāĒśĻß
B.×ų±źµćpŠĪ³ÉµÄČÜŅŗŹĒAgClµÄ²»±„ŗĶČÜŅŗ
C.mµćŹĒŌŚĖ®ÖŠ¼ÓČė×ćĮæµÄAgBrŠĪ³ÉµÄ±„ŗĶČÜŅŗ
D.nµć±ķŹ¾ÓɹżĮæµÄKIÓėAgNO3·“Ó¦²śÉśAgI³Įµķ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æamolFeSÓėbmolFeOĶ¶ČėVLcmol/LµÄHNO3ČÜŅŗ£Ø¹żĮ棩֊£¬³ä·Ö·“Ó¦£¬²śÉśĘųĢåĪŖNO£¬Ōņ·“Ó¦ŗóČÜŅŗÖŠNO3©µÄĮæĪŖ£Ø £©
A.62£Øa+b£©g
B.186£Øa+b£©g
C.£ØcV© ![]() £©mol
£©mol
D.£ØcV© ![]() £©mol
£©mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°×Į×ÓėŃõæÉ·¢ÉśČēĻĀ·“Ó¦£ŗP4+5O2ØTP4O10 £® ŅŃÖŖ¶ĻĮŃĻĀĮŠ»Æѧ¼üŠčŅŖĪüŹÕµÄÄÜĮæ·Ö±šĪŖ£ŗP©P£ŗa kJmol©1”¢P©O£ŗb kJmol©1”¢P=O£ŗc kJmol©1”¢O=O£ŗd kJmol©1 £® øł¾ŻĶ¼Ź¾µÄ·Ö×Ó½į¹¹ŗĶÓŠ¹ŲŹż¾Ż¹ĄĖćøĆ·“Ó¦µÄ”÷H£¬ĘäÖŠÕżČ·µÄŹĒ£Ø £© 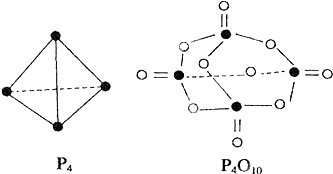
A.£Ø6a+5d©4c©12b£©kJmol©1
B.£Ø4c+12b©6a©5d£©kJmol©1
C.£Ø4c+12b©4a©5d£©kJmol©1
D.£Ø4a+5d©4c©12b£©kJmol©1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄA”¢B”¢C”¢D”¢E”¢FĮłÖÖŌŖĖŲ£®ĘäÖŠAµÄ»łĢ¬Ō×ÓÓŠ3øö²»Ķ¬µÄÄܼ¶£¬ø÷Äܼ¶ÖŠµÄµē×ÓŹżĻąµČ£»CµÄ»łĢ¬Ō×Ó2pÄܼ¶ÉĻµÄĪ“³É¶Ōµē×ÓŹżÓėAŌ×ÓµÄĻąĶ¬£»DĪŖĖüĖłŌŚÖÜĘŚÖŠŌ×Ó°ė¾¶×ī“óµÄÖ÷×åŌŖĖŲ£»EŗĶCĪ»ÓŚĶ¬Ņ»Ö÷×壬FµÄŌ×ÓŠņŹżĪŖ29£®
£Ø1£©FŌ×Ó»łĢ¬µÄĶāĪ§ŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ £®
£Ø2£©ŌŚA”¢B”¢CČżÖÖŌŖĖŲÖŠ£¬µŚŅ»µēĄėÄÜÓÉŠ”µ½“óµÄĖ³ŠņŹĒ£ØÓĆŌŖĖŲ·ūŗÅ»Ų“š£©£®
£Ø3£©ŌŖĖŲBµÄ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄ·Šµć£ØøßÓŚ£¬µĶÓŚ£©ŌŖĖŲAµÄ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄ·Šµć£¬ĘäÖ÷ŅŖŌŅņŹĒ £®
£Ø4£©ÓÉA”¢B”¢CŠĪ³ÉµÄĄė×ÓCAB©ÓėAC2»„ĪŖµČµē×ÓĢ壬ŌņCAB©µÄ½į¹¹Ź½ĪŖ £®
£Ø5£©ŌŚŌŖĖŲAÓėEĖłŠĪ³ÉµÄ³£¼ū»ÆŗĻĪļÖŠ£¬AŌ×Ó¹ģµĄµÄŌÓ»ÆĄąŠĶĪŖ £®
£Ø6£©ÓÉB”¢C”¢DČżÖÖŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļ¾§ĢåµÄ¾§°ūČēĶ¼ĖłŹ¾£¬ŌņøĆ»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖ £® 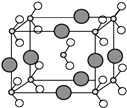
£Ø7£©FCŌŚ¼ÓČČĢõ¼žĻĀČŻŅ××Ŗ»ÆĪŖF2C£¬“ÓŌ×Ó½į¹¹µÄ½Ē¶Č½āŹĶŌŅņ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com