

·ÖĪö £Ø1£©ŹµŃéŹŅĶس£ÓĆ¼ÓČČĒāŃõ»ÆøĘÓėĀČ»Æļ§µÄ»ģŗĻ¹ĢĢåµÄ·½·ØÖĘČ”°±Ęų£¬ŌŚ¼ÓČČĢõ¼žĻĀ£¬ĀČ»Æļ§ŗĶĒāŃõ»ÆøĘ·“Ӧɜ³ÉĀČ»ÆøĘ”¢°±ĘųŗĶĖ®£»
£Ø2£©°±ĘųÓŠ“Ģ¼¤ŠŌĘųĪ¶£¬ÄÜĪŪČ¾“óĘų£¬×°ÖĆÖŠĆŽ»ØÄÜ·ĄÖ¹¹ÜÄŚĘųĢåÓėæÕĘų¶ŌĮ÷£¬¼õÉŁ°±Ęų¶Ō“óĘųµÄĪŪČ¾£¬±ćÓŚŹÕ¼Æ“æµÄ°±Ęų£»
£Ø3£©°±ĘųŗĶĖ®·“Ӧɜ³É°±Ė®£¬°±Ė®³Ź¼īŠŌ£¬øł¾Ż°±Ė®µÄŠŌÖŹČ·¶Ø¼ģŃé·½·Ø£»
£Ø4£©ĪŽÉ«·ÓĢŖŹŌŅŗÓö¼ī±äŗģÉ«£¬¼«Ņ×ČÜÓŚĖ®µÄĘųĢåÄÜŠĪ³ÉÅēČŖ£»
£Ø5£©°±Ęų¼«Ņ×ČÜÓŚĖ®£¬øł¾ŻC=$\frac{n}{v}$·ÖĪö£®
½ā“š ½ā£ŗ£Ø1£©°±ŃĪŗĶ¼ī·“Ӧɜ³É°±ĘųŗĶĖ®£¬ŹµŃéŹŅÓĆĒāŃõ»ÆøĘŗĶĀČ»Æļ§ŌŚ¼ÓČČĢõ¼žĻĀ·“Ó¦Öʱø°±Ęų£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖCa£ØOH£©2+2NH4Cl$\frac{\underline{\;\;”÷\;\;}}{\;}$CaCl2+2NH3”ü+2H2O£¬
¹Ź“š°øĪŖ£ŗCa£ØOH£©2+2NH4Cl $\frac{\underline{\;\;”÷\;\;}}{\;}$CaCl2+2NH3”ü+2H2O£»
£Ø2£©°±ĘųÓŠ“Ģ¼¤ŠŌĘųĪ¶£¬ÄÜĪŪČ¾“óĘų£¬ĪŖ·ĄÖ¹¹ÜÄŚĘųĢåÓėæÕĘų¶ŌĮ÷£¬¼õÉŁ°±Ęų¶Ō“óĘųµÄĪŪČ¾£¬±ćÓŚŹÕ¼Æ“æµÄ°±Ęų£¬ÓĆĆŽ»ØČūŌŚŹŌ¹ÜæŚ£¬
¹Ź“š°øĪŖ£ŗ·ĄÖ¹¹ÜÄŚĘųĢåÓėæÕĘų¶ŌĮ÷£¬¼õÉŁ°±Ęų¶Ō“óĘųµÄĪŪČ¾£¬±ćÓŚŹÕ¼Æ“æµÄ°±Ęų£»
£Ø3£©°±ĘųŗĶĖ®·“Ӧɜ³É°±Ė®£¬°±Ė®µēĄė³öļ§øłĄė×ÓŗĶĒāŃõøłĄė×Óµ¼ÖĀ°±Ė®³Ź¼īŠŌ£¬ŗģÉ«ŹÆČļŹŌÖ½Óö¼ī±äĄ¶É«£¬ĖłŅŌæÉŅŌÓĆŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½¼ģŃé°±Ęų£¬
¹Ź“š°øĪŖ£ŗÓĆŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½ææ½üĘææŚ£¬Čō±äĄ¶É«£¬ĖµĆ÷ŹÕ¼ÆĀśĘ棻
£Ø4£©ĪŽÉ«·ÓĢŖÓö¼ī±äŗģÉ«£¬øł¾ŻĶ¼BÅēČŖŹµŃéµÄ×°ÖĆ½ųŠŠŹµŃ飬¹Ū²ģµ½ŠĪ³ÉĆĄĄöµÄŗģÉ«ÅēČŖ£¬Ōņ°±ĘųµÄĖ®ČÜŅŗ³Ź¼īŠŌ£¬°±Ęų¼«Ņ×ČÜÓŚĖ®¶ųŠĪ³ÉŃ¹Ēæ²ī£¬µ¼ÖĀŠĪ³ÉÅēČŖ£¬
¹Ź“š°øĪŖ£ŗŠĪ³ÉĆĄĄöµÄŗģÉ«ÅēČŖ£»¼«Ņ×ČÜÓŚĖ®ŗĶČÜÓŚĖ®ŗóČÜŅŗ³Ź¼īŠŌ£»
£Ø5£©ÉčÉÕĘæµÄĢå»żĪŖV£¬ĘųĢåĦ¶ūĢå»żĪŖVm£¬Ōņ°±Ė®µÄĪļÖŹµÄĮæÅضČC=$\frac{n}{v}$=$\frac{V}{\frac{Vm}{V}}$=$\frac{1}{{V}_{m}}$£¬ÓėĘųĢåµÄĢå»żĪŽ¹Ų£¬Ņņ“Ė¼××éĶ¬Ń§ĖłµĆ°±Ė®µÄĪļÖŹµÄĮæÅØ¶ČµČÓŚŅŅ×éĶ¬Ń§ĖłµĆ°±Ė®µÄĪļÖŹµÄĮæµÄÅØ¶Č£¬
¹Ź“š°øĪŖ£ŗµČÓŚ£®
µćĘĄ ±¾Ģāæ¼²éĮĖ°±ĘųµÄŹµŃéŹŅÖĘ·Ø”¢ŹÕ¼Æ·½·Ø”¢°±ĘųµÄŠŌÖŹµČÖŖŹ¶µć£¬Ć÷Č·ŹµŃéŌĄķŹĒ½ā±¾Ģā¹Ų¼ü£¬øł¾Ż°±ĘųµÄČܽāŠŌ¼°ĆܶČČ·¶ØŹÕ¼Æ·½·Ø£¬ÖŖµĄŠĪ³ÉÅēČŖµÄĢõ¼ž£ŗÖ»ŅŖĘųĢ弫Ņ×ČÜÓŚøĆČÜŅŗ¾ĶÄÜŠĪ³ÉÅēČŖ£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ĪŖÖ¤Ć÷·Ē½šŹōŠŌĒæČõ£ŗS£¾C£¾Si | |
| B£® | 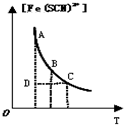 ±ķŹ¾æÉÄę·“Ó¦Fe3+£Øaq£©+SCN-£Øaq£©?Fe£ØSCN£©2+£Øaq£©Ę½ŗāŹ±£¬ĪļÖŹµÄĮæÅضČ[Fe£ØSCN£©2+]ÓėĪĀ¶ČTµÄ¹ŲĻµ£¬·“Ó¦“¦ÓŚDµćŹ±£¬Ņ»¶ØÓŠV£ØÕż£©£¼V£ØÄę£© | |
| C£® | 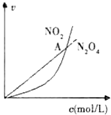 ±ķŹ¾ŗćĪĀŗćČŻĢõ¼žĻĀ·¢ÉśµÄæÉÄę·“Ó¦2NO2£Øg£©?N2O4£Øg£©ÖŠ£¬ø÷ĪļÖŹµÄÅضČÓėĘäĻūŗÄĖŁĀŹÖ®¼äµÄ¹ŲĻµ£¬ĘäÖŠ½»µćA¶ŌÓ¦µÄדĢ¬ĪŖ»ÆŃ§Ę½ŗāדĢ¬ | |
| D£® | 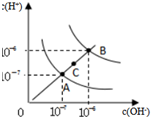 ĪŖĖ®µÄµēĄėĘ½ŗāĒśĻßĶ¼£¬Čō“ÓAµćµ½Cµć£¬æÉŌŚĖ®ÖŠ¼ÓČėŹŹĮæNaOH¹ĢĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ¼ī½šŹōŌŖĖŲµÄŃōĄė×ÓĖęŗĖµēŗÉŹżŌö¼Ó£¬Ńõ»ÆŠŌ½„Čõ¶ų»¹ŌŠŌ½„Ēæ | |
| B£® | ¼ī½šŹōŌŖĖŲµÄŌ×Ó°ė¾¶Ō½“ó£¬Ō½Ņ׏§µē×Ó£¬Ę䵄֏»¹ŌŠŌŌ½Ēæ | |
| C£® | ĖęŗĖµēŗÉŹżŌö¶ą£¬¼ī½šŹōµ„ÖŹµÄČŪµćŅ»¶Ø½„µĶ£¬ĆܶČŅ»¶Ø½„“ó | |
| D£® | ¼ī½šŹōµ„ÖŹµÄ½šŹōŠŌĒ棬¾łŅ×ÓėCl2”¢O2”¢N2µČ·¢Éś·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µĪ¶ØĒ°ŠčŅŖ¼ģ²éµĪ¶Ø¹ÜŹĒ·ńĀ©Ė® | |
| B£® | ÓƶŌÓ¦¼ÓČėµÄČÜŅŗČóĻ“µÄŅĒĘ÷ÓŠ£ŗĖįŹ½µĪ¶Ø¹Ü”¢×¶ŠĪĘæ | |
| C£® | µĪ¶Ø¹Ü£Ø×°±ź×¼ČÜŅŗ£©ŌŚµĪ¶ØĒ°¼ā×ģ“¦ÓŠĘųÅŻ£¬µĪ¶ØÖÕĮĖĪŽĘųÅŻ£¬»įŹ¹µĪ¶Ø½į¹ūĘ«øß | |
| D£® | ÓĆŅŃÖŖÅضČŃĪĖįµĪ¶ØĪ“ÖŖÅØ¶ČµÄNaOHČÜŅŗ£¬ÖÕµć¶ĮŹżŹ±ø©ŹÓµĪ¶Ø¹ÜµÄæĢ¶Č£¬»įŌģ³É¼ĘĖćֵʫµĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| ŠņŗÅ | CaCO3/mol | CaO/mol | CO2/mol |
| A | 0.02 | 0.02 | 0.05 |
| B | 0.02 | 0.02 | 0.03 |
| C | 0.02 | 0.02 | 0.01 |
| D | 0.02 | 0 | 0.05 |
| E | 0.02 | 0.02 | 0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| µĪ¶Ø“ĪŹż | “ż²āČÜŅŗµÄĢå»ż/mL | ±ź×¼ČÜŅŗµÄĢå»ż | |
| µĪ¶ØĒ°æĢ¶Č/mL | µĪ¶ØŗóæĢ¶Č/mL | ||
| 1 | 25.00 | 1.05 | 21.04 |
| 2 | 25.00 | 1.50 | 24.50 |
| 3 | 25.00 | 0.20 | 20.21 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com