
| A. | 0.5mol | B. | 0.25mol | C. | 0.1mol | D. | 0.125mol |
分析 标况下5.6L氢气的物质的量=$\frac{5.6L}{22.4L/mol}$=0.25mol,故12g金属提供的电子为0.25mol×2=0.5mol,金属Mg、Zn、Fe与硫酸反应都表现为+2价,利用电子转移守恒计算三种金属的物质量之和.
解答 解:标准状况下为5.6L气体的物质的量为$\frac{5.6L}{22.4L/mol}$=0.25mol,
金属Mg、Zn、Fe与硫酸反应都表现为+2价,利用电子转移守恒计算三种金属的物质量之和,
故有2n(Mg)+2n(Zn)+2n(Fe)=2n(H2),
即n(Mg)+n(Zn)+n(Fe)=n(H2)=0.25mol,
故选B.
点评 本题考查混合物的有关计算,难度中等,可以利用方程式判断金属与氢气的物质的量关系.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:选择题
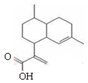
| A. | 青蒿素分子式为:C15H20O2 | |
| B. | 1 mol青蒿酸可与3 mol H2发生加成反应 | |
| C. | 在一定条件,可与乙醇发生酯化反应 | |
| D. | 能使溴水褪色,不能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中可能发生反应Z2+2A2+=2A3++2Z- | |
| B. | Z2在①③反应中作还原剂 | |
| C. | 氧化性强弱顺序为XO4->Z2>B2>A3+ | |
| D. | X2+是XO4-的还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:NH3>H2O>HF | B. | 熔点:金刚石>碳化硅>晶体硅 | ||
| C. | 硬度:白磷>冰>二氧化硅 | D. | 熔点:SiI4<SiBr4<SiCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
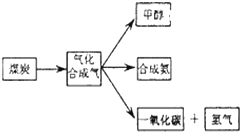
| 物质 | H2 | CO | CH3OH |
| 浓度(mol/L) | 0.2 | 0.1 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 密度小 | B. | 强度高 | C. | 不易生锈 | D. | 导电性好 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
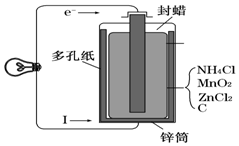 某学校设计了一节实验活动课,让学生从废旧干电池回收碳棒、锌皮、MnO2、NH4Cl、ZnCl2等物质,整个实验过程如下,请回答有关问题.
某学校设计了一节实验活动课,让学生从废旧干电池回收碳棒、锌皮、MnO2、NH4Cl、ZnCl2等物质,整个实验过程如下,请回答有关问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe与S混合加热生成FeS2 | |
| B. | 向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ | |
| C. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| D. | Fe在足量Cl2中燃烧生成FeCl2和FeCl3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com