
下列叙述正确的是 ( )。
A.原子晶体中只存在非极性共价键
B.干冰升华时,分子内共价键会发生断裂
C.由原子构成的晶体可以是原子晶体,也可以是分子晶体
D.只要含有金属阳离子的晶体就一定是离子晶体
科目:高中化学 来源: 题型:
已知:
①C(s)+1/2O2(g)===CO(g) ΔH1=-110.35 kJ·mol-1
②CO(g)+1/2O2(g)===CO2(g) ΔH2=-282.57 kJ·mol-1
③C(s)+O2(g)===CO2(g) ΔH3
则ΔH3等于( )
A.+172.22 kJ·mol-1 B.-172.22 kJ·mol-1
C.+392.92 kJ·mol-1 D.-392.92 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于粒子结构的描述不正确的是 ( )。
A.H2S 和 NH3 均是价电子总数为8的极性分子
B.HS -和 HCl 均是含一个极性键的 18 电子粒子
C.CH2Cl2 和 CCl4 均是四面体构型的非极性分子
D.NCl3 是含极性键的极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)请写出元素N的基态原子电子排布式:____________________________。
(2)元素B、G形成的单质熔点更高的是________(填化学式),原因是________
________________________________________________________________。
(3)ME2L2常温下为深红色液体,能与 CCl4、CS2 等互溶,据此可判断 ME2L2 是________(填“极性”或“非极性”)分子。根据等电子原理:NO 中氮原子的杂化类型是________;1 mol NO
中氮原子的杂化类型是________;1 mol NO 中含有 π 键的数目为__________。
中含有 π 键的数目为__________。
(4)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有________(填序号),CS2分子的立体构型是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
高温下,超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价。如右图所示为超氧化钾晶体的一个晶胞,则下列说法正确的是( )。
A.超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O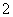
B.晶体中每个K+周围有8个O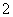 ,每个O
,每个O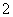 周围有8个K+
周围有8个K+
C.晶体中与每个K+距离最近的K+有8个
D.晶体中与每个K+距离最近的K+有6个
查看答案和解析>>
科目:高中化学 来源: 题型:
为了探究金属腐蚀的条件和快慢,某课外学习小组用不同的细金属丝将三根大小相同的普通铁钉分别固定在如图所示的三个装置内,并将这些装置在相同的环境中放置相同的一段时间,下列对实验结果的描述不正确的是( )

A.实验结束时,装置甲左侧的液面一定会下降
B.实验结束时,装置甲左侧的液面一定比装置乙的低
C.实验结束时,铁钉b腐蚀最严重
D.实验结束时,铁钉c几乎没有被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
为省药品和时间,甲、乙、丙三位同学用铜片、锌片、稀硫酸、CuSO4溶液(直流电源、石墨电极、导线、烧杯、试管等中学化学常见的药品和仪器用品)以巧妙的构思“接力”的方式,设计了比较铜与锌金属活动性相对强弱的系列实验。试填写下列空白:
(1)甲同学分别将一小片铜片、锌片置于烧杯底部(铜与锌不接触),小心向烧杯中加入稀硫酸,观察到的现象是___________________________________________________
________________________________________________________________________。
甲同学的设计思路是__________________________________________________
________________________________________________________________________。
(2)乙同学接着甲的实验,向烧杯中滴加________溶液,进而观察到的现象是________________________________________________________________________
________________________________________________________________________。
乙同学判断出锌、铜金属活动性相对强弱,所依据的原理是
________________________________________________________________________
________________________________________________________________________。
(3)丙同学使用直流电源、石墨电极组装好电解装置,向乙同学实验后的溶液中补充了必要的试剂(作为电解液),反应在调控下随即开始,实验中有关的化学反应方程式为________________________________________________________________________
________________________________________________________________________。
获得的实验明显现象是_______________________________________________
________________________________________________________________________。
(4)请你再单独设计一个简单的实验(试剂、仪器自选),探究和证实锌和铜的金属活动性的相对强弱(简要说明操作和现象)________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A+、B+、C-、D、E五种粒子(分子或离子),它们都分别含有10个电子,已知它们有如下转化关系:
①A++C-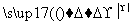 D+E↑
D+E↑
②B++C-—→2D
(1)写出①的离子方程式:_____________________________;
写出②的离子方程式:_________________________________。
(2)除D、E外,请再写出两种含10个电子的分子:________________________________________________________。
(3)除A+、B+外,请再写出两种含10个电子的阳离子:
__________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com