
| A. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 醋酸溶液中加入烧碱溶液:H++OH-═H2O | |
| C. | Ba(OH)2与 H2SO4反应到恰好沉淀完全:Ba2++OH-+SO42-+H+═BaSO4↓+H2O | |
| D. | 向澄清的石灰水中滴入少量碳酸氢钠溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
分析 A.碳酸钙为难溶物,离子方程式中不能拆开;
B.醋酸为弱酸,离子方程式中醋酸需要保留分子式;
C.氢离子、氢氧根离子的化学计量数错误,不满足硫酸、氢氧化钡的化学式组成;
D.碳酸氢钠少量,反应生成碳酸钙沉淀、碳酸氢钠和水.
解答 解:A.碳酸钙不能拆开,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故A错误;
B.醋酸溶液中加入烧碱溶液,反应生成醋酸钠和水,醋酸不能拆开,正确的离子方程式为:+OH-+CH3COOH=H2O+CH3COO-,故B错误;
C.Ba(OH)2与 H2SO4反应到恰好沉淀,反应生成硫酸钡沉淀和水,正确的离子方程式为:Ba2++2OH-+SO42-+2H+═BaSO4↓+2H2O,故C错误;
D.向澄清的石灰水中滴入少量碳酸氢钠溶液,反应的离子方程式为:Ca2++OH-+HCO3-═CaCO3↓+H2O,故D正确;
故选D.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度不大,注意掌离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 +3Br2→
+3Br2→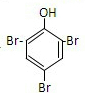 +3HBr
+3HBr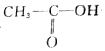 +H-O-CH2CH3$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O
+H-O-CH2CH3$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O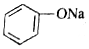 +CO2+H2O→C6H5OH+NaHCO3.
+CO2+H2O→C6H5OH+NaHCO3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
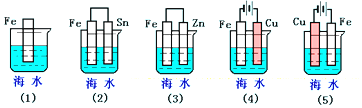
| A. | (5)(2)(1)(3)(4) | B. | (2)(5)(3)(4)(1) | C. | (5)(3)(4)(1)(2) | D. | (1)(5)(3)(4)(2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气在氯气中安静燃烧,发出苍白色火焰,瓶口出现的“雾气”是盐酸小液滴 | |
| B. | 漂白粉溶液中滴入少量盐酸,可增强其漂白效果 | |
| C. | 钠在空气中燃烧,产生黄色火焰,生成白色的Na2O的固体 | |
| D. | 铁丝在氯气中燃烧,生产棕红色的烟,氯化铁的水溶液呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠加入到紫色石蕊试液中,紫色石蕊先变红后褪色且有气泡产生 | |
| B. | 冷的浓硫酸和浓硝酸都可以用铝、铁的容器盛装 | |
| C. | 硅、氯、硫、氮、钠元素在自然界只有化合态没有游离态 | |
| D. | 浓硝酸有氧化性,稀硝酸没有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时PbO2发生氧化反应 | |
| B. | 充电时电解质溶液的质量减少 | |
| C. | 放电时的负极反应式为Pb+SO42--2e-=PbSO4 | |
| D. | 充电时的阴极反应式为PbSO4+2H2O-2e-=PbO2+SO42-+4H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com