
| A. | Fe(OH)2、Fe(OH)3;Fe3O4 | B. | Fe(OH)2;FeO | ||
| C. | Fe(OH)2、Fe(OH)3;Fe2O3 | D. | Fe2O3;Fe(OH)3 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等浓度CH3COOH溶液与NH3•H2O溶液等体积混合后,存在c(NH4+)+c(H+)=c(CH3COO-)+c(OH-) | |
| B. | 等浓度的HCl溶液与CH3COOH溶液中c(H+)也相同 | |
| C. | 向20mLHCl溶液中加入10mL同一浓度的HCl溶液时,其pH会改变 | |
| D. | 等浓度的CH3COOH溶液和NaOH溶液等体积混合后,溶液显中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 用如图所示装置测定氮肥[NH4HCO3中含(NH4)2CO3]中NH4HCO3的质量分数(不考虑铵盐溶液分解).
用如图所示装置测定氮肥[NH4HCO3中含(NH4)2CO3]中NH4HCO3的质量分数(不考虑铵盐溶液分解).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
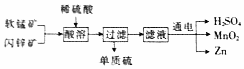 工业上可用软锰矿(主要成分MnO2)和闪锌矿(主要成分为ZnS)制备干电池中所需的MnO2和Zn,其工艺流程如图所示,下列说法中错误的是( )
工业上可用软锰矿(主要成分MnO2)和闪锌矿(主要成分为ZnS)制备干电池中所需的MnO2和Zn,其工艺流程如图所示,下列说法中错误的是( )| A. | 上述流程中锰元素的价态没有变化 | |
| B. | 上述流程中的硫酸可循环利用 | |
| C. | 通电过程中,生成Zn单质时发生还原反应 | |
| D. | 通电过程中,阳极的电极反应式为Mn2+-2e-+2H2O═MnO2+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BeCl2溶液pH<7,将其蒸干、灼烧后可得残留物BeCl2 | |
| B. | BeCl2水溶液的导电性强,BeCl2一定是离子晶体 | |
| C. | Be(OH)2能溶于盐酸,不能溶于NaOH溶液 | |
| D. | Na2BeO2溶液pH>7,将其蒸干、灼烧后可得残留物Na2BeO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 固体SiO2一定是晶体 | |
| B. | 晶体有固定的组成,非晶体没有固定的组成 | |
| C. | 晶体内部的微粒按一定规律呈周期性有序排列 | |
| D. | 晶体的基本结构单元(晶胞)全部是平行六面体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com