
| A、木炭燃烧 |
| B、生石灰与水反应 |
| C、酸碱中和反应 |
| D、Ba(OH)2?8H2O晶体与NH4Cl晶体反应 |


科目:高中化学 来源: 题型:

| n(H2O) |
| n(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、按照系统命名法,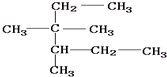 的名称为3,3,4-三甲基己烷 的名称为3,3,4-三甲基己烷 |
| B、乙醇、乙酸和乙酸乙酯可以用饱和Na2CO3溶液鉴别 |
| C、苯乙烯中所有原子可能共平面 |
D、1.0mol的 与NaOH溶液和Br2反应时,分别需要消耗NaOH 5.0mol和Br2 3.0mol 与NaOH溶液和Br2反应时,分别需要消耗NaOH 5.0mol和Br2 3.0mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定产生BaSO3沉淀 |
| B、一定产生BaSO4沉淀 |
| C、产生的不全是BaSO4沉淀 |
| D、一定有SO3逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 | B、2 | C、3 | D、4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、吸热反应一定要加热才能发生 |
| B、在5mL 0.1mol?L-1的KI溶液中加入5滴0.1mol?L-1 FeCl3溶液,充分震荡后,取少量混合液液加入几滴KSCN溶液,溶液显红色 |
| C、一定温度下,在某容器中进行可逆反应:C(s)+H2O(g)?CO(g)+H2(g),只要增大压强,反应速率一定加快 |
| D、电解氯化钠溶液可制得金属钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H<0且参与反应的高氯酸钾越多,其值越小 |
| B、在该热电池中,铁为负极,发生还原反应 |
| C、正极反应式为KClO4(s)+8e-═KCl(s)+4O2-(l) |
| D、生成1mol FeO转移8mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com