
【题目】硝基苯是一种重要的化工原料,其制备原理是:
![]()
![]()
在温度稍高的情况下会生成副产物间二硝基苯: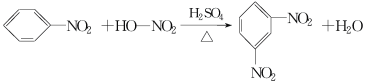

请将下列制备硝基苯的实验内容填写完整:
(1)混酸的配制:取100 mL烧杯,用浓硫酸20 mL、浓硝酸18 mL配制混酸,其操作过程为__________________________________
(2)安装反应装置:按图所示安装实验装置,在这个实验中冷凝管的作用是 _
(3)反应步骤:①把18 mL的苯加入到三颈瓶中,将混酸加入到分液漏斗中,逐滴滴加混酸,边滴加边搅拌,这样做的目的是____________________________ _
②混酸滴加完毕后,在加热搅拌的条件下反应半小时。控制加热温度的方法是___ ____ 。
③分离和提纯:除去产物中没有反应的酸,可在产物中加入碱溶液,然后用分液漏斗分液,______层物质为粗产品。除去硝基苯中没有反应的苯和生成的副产物的简便方法是(填方法名称)__________。
【答案】(1)在100 mL 的烧杯中先加入18 mL 浓硝酸,然后缓慢加入20 mL 浓硫酸,不断搅拌,冷却到50~60℃
(2)冷凝回流,防止苯和硝酸挥发(或者回答提高原料的利用率也可)
(3)①防止反应进行得过快,使温度升高得过快,增加反应的副产物②水浴加热 ③下 蒸馏
【解析】
试题分析:(1)混酸的配制过程为在100 mL 的烧杯中先加入18 mL 浓硝酸,然后缓慢加入20 mL 浓硫酸,不断搅拌,冷却到50~60℃;
(2)制备硝基苯的反应为放热反应,硝酸、苯都易挥发,所以为了提高反应物的转化率,对反应物要冷凝回流,所以冷凝管的作用是冷凝回流,防止苯和硝酸挥发;
(3)①制备硝基苯的反应为放热反应,反应温度升高快,会发生副反应生成副产物间二硝基苯,所以逐滴滴加混酸,边滴加边搅拌的目的是防止反应进行得过快,使温度升高得过快,增加反应的副产物;
②反应要控制在50~60℃,可以用水浴加热;
③硝基苯的密度大于水,所以粗产品在下层;苯和硝基苯及间二硝基苯互溶但它们的沸点不同,所以除去硝基苯中没有反应的苯和生成的副产物的方法是蒸馏。


科目:高中化学 来源: 题型:
【题目】取一小块金属钠,放在燃烧匙里加热,下列实验现象描述不正确的是( )
A. 燃烧后得白色固体B. 燃烧时火焰为黄色
C. 燃烧后生成淡黄色固体物质D. 金属先熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟。如图是钒电池基本工作原理示意图:

请回答下列问题:
(1)钒电池是以溶解于一定浓度硫酸溶液中的不同价态的钒离子(V2+、V3+、VO2+、VO![]() )为正极和负极电极反应的活性物质,电池总反应为 V2++VO
)为正极和负极电极反应的活性物质,电池总反应为 V2++VO![]() +2H+
+2H+![]() VO2++V3++H2O。放电时的正极反应式为______________________,充电时的阴极反应式为_____________。
VO2++V3++H2O。放电时的正极反应式为______________________,充电时的阴极反应式为_____________。
(2)钒电池基本工作原理示意图中“正极电解液”可能是________。
a.VO![]() 、VO2+混合液 b.V3+、V2+混合液 c.VO
、VO2+混合液 b.V3+、V2+混合液 c.VO![]() 溶液
溶液
d.VO2+溶液 e.V3+溶液 f.V2+溶液
Ⅱ、氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2]的碱性溶液制氢气的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。

(1)图1中N型半导体为__________(填“正极”或“负极”)
(2)该系统工作时,A极的电极反应式为________________
(3)若A极产生7.00gN2,则此时B极产生________L H2(标况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 氢氧化钠的摩尔质量为40 g
B. 氢原子的摩尔质量是1 g·mol-1
C. 1 mol水的质量是18 g·mol-1
D. 二氧化碳的摩尔质量为44 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学实验的说法正确的是
A. 测任何溶液pH时都可使用广泛pH试纸或精密pH试纸
B. 无水氯化钙可干燥CO2、Cl2、NH3、CO等常见气体
C. 用酒精灯加热烧瓶、烧杯、试管时都需要垫石棉网
D. 萃取、过滤都是利用物质的物理性质进行分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017届湖南省怀化市高三上学期期中质检化学试卷】CO2是目前最主要的温室气体,减小CO2的排放并用来制造有价值的化学用品是目前的研究目标。
(1)利用CO2与CH4生产合成气(CO、H2):
已知:CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) ΔH=-890.3 KJ·mol-1
CO2(g)+2H2O(g) ΔH=-890.3 KJ·mol-1
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH=+2.8 KJ·mol-1
CO2(g)+H2(g) ΔH=+2.8 KJ·mol-1
2CO(g)+O2(g)![]() 2CO2(g) ΔH=-566.0 KJ·mol-1
2CO2(g) ΔH=-566.0 KJ·mol-1
反应CO2(g)+CH4(g)![]() 2CO(g)+2H2(g) ΔH= ____________。
2CO(g)+2H2(g) ΔH= ____________。
②250℃时,以镍合金为催化剂,向体积为4 L的密闭容器中通入6 mol CO2、6 mol CH4,开始发生如下反应:CO2(g)+CH4(g)![]() 2CO(g)+2H2(g)。经过一段时间达到平衡,平衡体系中各组分体积分数(某一成分物质的量占总气体物质的量的百分数)如下表:
2CO(g)+2H2(g)。经过一段时间达到平衡,平衡体系中各组分体积分数(某一成分物质的量占总气体物质的量的百分数)如下表:
物质 | CH4 | CO2 | CO | H2 |
体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
此温度下该反应的平衡常数K=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同条件下,ag的A气体与bg的B气体占有相同体积。下列叙述错误的是 ( )
A. a∶b等于A与B的相对分子质量之比
B. a∶b等于等质量的A与B的分子数之比
C. a∶b等于同温同压下A与B的密度之比
D. b∶a等于同温同体积等质量的A与B的压强比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 ml 0.1 mol/L的ALCl3溶液与200 ml 0.3 mol/L的NaCl溶液中c(Cl-)之比为
A. 1:1 B. 1:2 C. 1:3 D. 3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着汽车数量的逐年增多,汽车尾气污染已成为突出的环境问题之一。反应:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是( )
2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是( )
A.提高尾气净化效率的最佳途径是研制高效催化剂
B.提高尾气净化效率的常用方法是升高温度
C.装有尾气净化装置的汽车排出的气体中不再含有NO或CO
D.570 K时及时抽走CO2、N2,平衡常数将会增大,尾气净化效率更佳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com