
| A. | 工业上常采用电解法冶炼Y 单质 | |
| B. | 气态氢化物的稳定性:H2W强于H2Z | |
| C. | 离子半径由大到小:Z2->X+>Y3+>W2- | |
| D. | W、X 形成的化合物中阴、阳离子个数比一定是1:2 |
分析 原子序数依次递增的4种短周期元素可形成简单离子 W2-,X+,Y3+,Z2-,则W、Z为第VIA,原子序数W小于Z,则W为O元素,Z为S元素,X化合价为+1价为第IA族的Na元素,Y为第IIIA族,原子序数大于Na,则Y为Al元素,结合元素化合物的性质分析.
解答 解:A.Y为Al元素,常用电解熔融的氧化铝的方法制备铝,故A正确;
B.元素的非金属性越强,其氢化物越稳定,非金属性:O大于S,则气态氢化物的稳定性:H2O强于H2S,故B正确;
C.电子层数越多离子半径越大,电子排布相同的离子,原子序数越大,离子半径越小,所以S2->O2->Na+>Al3+?,则Z2->W2-X+>Y3+?,故C错误;
D.W、X 形成的化合物为Na2O或Na2O2,阴、阳离子个数比一定是1:2,故D正确.
故选C.
点评 本题考查元素推断、元素周期律、元素化合物性质等,难度中等,侧重于考查学生的分析能力,推断元素是解题的关键,需要学生熟练掌握元素化合物性质.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用石墨电极电解FeCl3溶液,阴极反应:2Fe3++6H2O+6e-=2Fe(OH)3↓+3H2↑ | |
| B. | 1 mol•L-1的NH4Cl溶液中含有NH4+的数目一定小于NA | |
| C. | NaHCO3溶液加水稀释,$\frac{c(N{a}^{+})}{c(HC{{O}_{3}}^{-})}$的比值保持增大 | |
| D. | 将带有相反电荷的胶体混合,一定会出现胶体聚沉现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、ClO-、Cl- | B. | Mg2+、Na+、SO42-、Cl- | ||
| C. | Ca2+、HCO3-、NO3-、K+ | D. | Na+、Cu2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 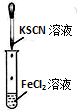 装置溶液变红色 | |
| B. | 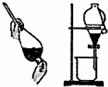 装置可用于分离乙醇和水的混合物 | |
| C. | 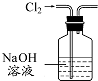 装置可除去Cl2中含有的少量HCl气体 | |
| D. | 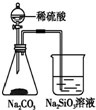 装置所示实验可验证酸性:H2SO4>H2CO3>H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
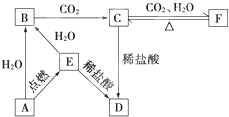
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤燃烧是化学能转化为光能的过程 | |
| B. | 1 mol 甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 | |
| C. | HCl 和 NaOH 反应的中和热△H=-57.3 kJ•mol-1,则 H2SO4 和 Ca(OH)2 反应中和热△H=2×(-57.3)kJ•mol-1 | |
| D. | 反应 H2(g)+F2(g)═2HF(g);△H=-270 kJ•mol-1说明在相同条件下,1 mol 氢气与 1 mol 氟气的能量总和大于2 mol 氟化氢气体的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某物质灼烧时,焰色反应为黄色,则该物质一定是金属钠 | |
| B. | 与水反应生成酸的物质就是酸性氧化物 | |
| C. | 胶体:分散质颗粒直径在1nm~100nm之间的分散系,能产生丁达尔效应 | |
| D. | 物质的量:衡量物质微粒个数的单位 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com