
分析 根据题目中的信息:“某银白色固体A在空气中点燃,火焰呈黄色,并生成淡黄色固体B”,“将A在空气中露置,最后变成白色固体C”,“将A、B投入水中都生成D;B与D分别与二氧化碳反应,都有生成E”,则推测A为钠,B过氧化钠,C为碳酸钠,D为氢氧化钠,代入检验符合题意.
解答 解:某银白色固体A在空气中点燃,火焰呈黄色,说明含钠元素,并生成淡黄色固体B为过氧化钠,则A为Na,将A在空气中露置,最后变成白色固体C,将A、B投入水中都生成D;B与D分别与二氧化碳反应,则推测A为钠,B过氧化钠,C为碳酸钠,D为氢氧化钠,
根据分析可知:A是Na;B是Na2O2 ;C是Na2CO3;D是NaOH,
B与H2O反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑,
B与CO2反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2↑.
A与H2O反应的化学方程式为:2Na+2H2O=2NaOH+H2↑,
故答案为:Na、Na2O2、Na2CO3、NaOH;2Na2O2+2H2O=4NaOH+O2↑;2Na2O2+2CO2=2Na2CO3+O2;2Na+2H2O=2NaOH+H2↑.
点评 本题考查了钠及其化合物性质,在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可,再根据推出的反应物、生成物书写化学方程式,题目难度不大.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:推断题
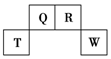 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等. .用化学方程式表示工业常用冶炼T单质的原理是2Al2O3(熔融)$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑.
.用化学方程式表示工业常用冶炼T单质的原理是2Al2O3(熔融)$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时的Cu为负极 | |
| B. | 充电时电解液的pH升高 | |
| C. | 充电时阳极电极反应为:PbSO4+2H2O-2e-═PbO2+4H++SO42- | |
| D. | 每消耗1molCu,电解质溶液中转移2mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com