
| A.Na+、Cu2+、SO42—、NH3·H2O |
| B.K+、Al3+、MnO4—、C2H5OH |
| C.K+、Cl—、NO3—、Fe2+ |
| D.Na+、NH4+、CH3COOH |
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源:不详 题型:单选题
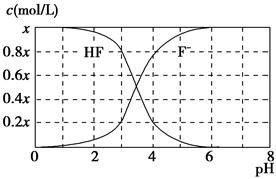
| A.当c(F-)>c(HF)时,溶液呈碱性 |
| B.当pH=2时,c(F-)<c(K+) |
| C.25 ℃时,氢氟酸的电离平衡常数为4×10-6 |
| D.当pH=5时,c(HF)+c(K+)+c(H+)-c(OH-)=x mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.向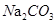 溶液通入 溶液通入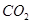 ,可使水解平衡: ,可使水解平衡: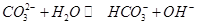 向正反应方向移动,则溶液pH增大 向正反应方向移动,则溶液pH增大 |
B.室温时,0.1mol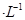 某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4 某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4 |
C.25℃时,pH=13的1.0 L Ba 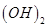 溶液中含有的 溶液中含有的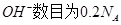 |
| D.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.无色的溶液中:Fe3+、K+、NO3-、Cl- |
| B.pH=13的溶液中:NH4+、Na+、SO42-、Cl- |
| C.含有大量Ba2+ 的溶液中:NH4+、Na+、Cl-、H+ |
| D.c(H+)=0.1 mol·L-1的溶液中:K+、I-、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.能使酚酞变红的溶液:Na+、Ba2+、NO3-、Cl- |
| B.含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、SO42- |
| C.能溶解Al(OH)3的溶液:NH4+、K+、SO42-、HCO3- |
| D.c(Al3+)="0.5" mol·L-1的溶液中:Na+、K+、[Al(OH)4]-、SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=0的溶液中:K+、Fe2+、C1-、NO3- |
| B.强碱性溶液中:Na+、K+、A1O2-、CO32- |
| C.c(H+)=c(OH-)的溶液中:Na+、Ba2+、C1-、SO42- |
| D.使蓝色石蕊试液变红的溶液中:Na+、K+、SO32-、HCO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+、Ba2+、OH—、Cl— | B.Na+、NH4+、OH—、HCO3— |
| C.NH4+、A13+、SiO32—、CO32ˉ | D.H+、Ag+、Cl—、ClO— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
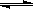 H++OH- KW=10-14 CH3COOH
H++OH- KW=10-14 CH3COOH 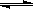 H++ CH3COO- Ka=1.8×10-5
H++ CH3COO- Ka=1.8×10-5| A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol·L-1 |
| B.若V1=V2,反应后溶液pH一定等于7 |
| C.若反应后溶液呈酸性,则V1一定大于V2 |
| D.若反应后溶液呈碱性,则V1一定小于V2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com