
| A、用烧杯给液态物质加热时,不用垫石棉垫 |
| B、加热蒸干AlCl3溶液得到Al2O3固体 |
| C、在用托盘天平称量固体药品时,药品放在右盘上 |
| D、如果未知溶液中滴加BaCl2溶液有白色沉淀生成,证明一定含有SO42-离子 |


科目:高中化学 来源: 题型:
| A、室温下,pH=1的盐酸中:Na+、Fe3+、NO3-、SO42- |
| B、强碱性溶液中:K+、Mg2+、Cl-、SO42- |
| C、含有Ca2+的溶液中:Na+、K+、CO32-、Cl- |
| D、由水电离产生的c(H+)=1×10-13mol/L的溶液中:Na+、K+、SiO32-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
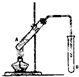 乙酸是实验室常用的化学药品之一.请回答下列问题:
乙酸是实验室常用的化学药品之一.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 增塑剂(DEHP)的结构简式如图所示,下列有关增塑剂的说法不正确的是( )
增塑剂(DEHP)的结构简式如图所示,下列有关增塑剂的说法不正确的是( )| A、DEHP的分子式为C24H35O4 |
| B、DEHP在碱性条件下能水解 |
C、DEHP可由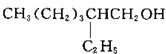 和 和 在高温与催化剂条件下制得 在高温与催化剂条件下制得 |
| D、DEHP不能用作食品添加剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有乙醇 |
| B、只有乙酸 |
| C、乙酸乙酯、乙醇、乙酸 |
| D、只有乙醇和乙酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 钢铁等铁制品是应用最广泛的金属材料,铁元素的单质及其化合物在元素化合物世界始终扮演着重要角色.
钢铁等铁制品是应用最广泛的金属材料,铁元素的单质及其化合物在元素化合物世界始终扮演着重要角色.| 1 |
| 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com