
【题目】将物质的量浓度相等的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液的pH随时间t变化的曲线如图所示,则下列说法中不正确的是
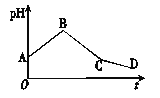
A. A点pH小于7是因为Cu2+水解使溶液显酸性
B. C点的pH比A点的pH小
C. BC段阳极产物是H2
D. CD段电解的物质是H2O
【答案】C
【解析】设CuSO4的和NaCl各1mol,由题意,结合图像可得,电解分3个阶段,第一阶段:阳极:1mol氯离子失1mol电子,阴极:0.5mol铜离子得1mol电子,因为溶液显酸性是铜离子水解的原因,所以铜离子减少,使溶液酸性减弱,pH值增大;第二阶段:阳极:1mol氢氧根离子失1mol电子(来源于水的电离),阴极:0.5mol铜离子得1mol电子,因为氢氧根离子消耗,所以水溶液中氢离子浓度增大,pH值迅速减小;第三阶段:阳极:氢氧根离子失电子,阴极:氢离子得电子,他们都来源于水的电离,但电解过程中水消耗了,使溶液中氢离子浓度增大,pH值减小;A项,A点为硫酸铜和NaCl混合溶液,其中硫酸铜为强酸弱碱盐,水解呈酸性,此时没有进行电解,所以pH小于7,故A正确;B项,A点因为铜离子部分水解而使溶液呈弱酸性,C点溶液中铜离子已全部被还原,此时溶液是硫酸钠和硫酸的混合溶液,溶液酸性增强,所以C点的pH比A点的pH小,故B正确;C项,由上述分析可知,整个过程中阳极先产生Cl2,后产生O2,故C错误;D项,由上述分析,CD段:阳极产生氧气,阴极产生氢气,相当于电解水,故D正确。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值.下列说法不正确的是( )
A.常温常压下,8 g O2含有4NA个电子
B.盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5 mol
C.常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
D.常温常压下,22.4 L的NO2和CO2混合气体含有2NA个O原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实现下列转化,必须加入氧化剂或还原剂的是( )
A. Cl2→HCl+HClO B. NH4+→NH3
C. NH3→NO D. CO2→CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA代表阿伏加德罗常数,下列表述正确的是
A.将NA个NH3分子气体溶于1L水中得到1mol·L-1的氨水
B.22.4L二氧化硫分子中电子总数约为32NA
C.1 mol Na与足量O2反应生成Na2O或Na2O2均失去NA个电子
D.各5.6 g铁分别与足量的盐酸、氯气反应,电子转移总数均为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质所配成的0.1 mol/L溶液中,离子浓度由大到小顺序排列正确的( )
A. NH4Cl:c(Cl-)>c(H+)>c(NH4+)>c(OH-)
B. Na2CO3:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
C. NaHCO3:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
D. ( NH4)2SO4:c(NH4+)>c(SO42-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验有几个不能达到实验目的是( )
(1)将![]() 与NaOH的醇溶液共热制备CH3CH=CH2
与NaOH的醇溶液共热制备CH3CH=CH2
(2)除去苯中的苯酚,先滴入适量的浓溴水,再过滤
(3)在一支盛有2mL 2%CuSO4溶液的试管中,滴入几滴10%的NaOH溶液,再加入1mL乙醛溶液,煮沸后可以看到有红色沉淀生成
(4)用溴的四氯化碳溶液吸收SO2气体.
A. 1个 B. 2个 C. 3个 D. 4个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】既可以用来鉴别乙烯和甲烷,又可以用来除去甲烷中混有的乙烯,得到纯净的甲烷的方法是
A. 与足量的溴水反应 B. 通过澄清石灰水 C. 酸性KMnO4溶液 D. 浓硫酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com