
分析 依据盖斯定律和热化学方程式计算得到所需的热化学方程式,利用热化学方程式的加减消去不需要的物质,注意加减时焓变随之变化.
解答 解:已知热化学方程式:2CO2(g)+2H2O(l)+2C5H10O4(s)═4(C3H6O3)+(s)+O2(g)+4e-△H═+1360kJ•mol-1 ①
12(C3H6O3)+(s)+12e-═C6H12O6(S,葡萄糖)+6C5H10O4(s)+3O2(g)△H=-1200kJ•mol-1②
根据盖斯定律,将①×3+②可得:6CO2(g)+6H2O(l)=C6H12O6(s)+6O2(g)△H=+2880 kJ•mol-1,
故答案为:6CO2(g)+6H2O(l)=C6H12O6(s)+6O2(g)△H=+2880 kJ•mol-1.
点评 本题涉及盖斯定律的应用,注意知识的迁移和应用是关键,难度中等.


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:选择题
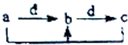 下表各组物质中,物质之间不能通过一步反应实现如图所示转化的( )
下表各组物质中,物质之间不能通过一步反应实现如图所示转化的( )| 物质 选项 | a | b | c | d |
| A | Al | Al(OH)3 | NaAlO2 | NaOH |
| B | C | CO | CO2 | O2 |
| C | NaOH | Na2CO3 | NaHCO3 | CO2 |
| D | AlCl3 | Al(OH)3 | NaAlO2 | NaOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
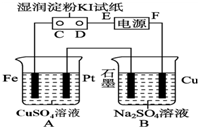 用如图所示的装置进行电解.通电一会儿,发现用NaCl溶液湿润的淀粉KI试纸的C端变为蓝色.
用如图所示的装置进行电解.通电一会儿,发现用NaCl溶液湿润的淀粉KI试纸的C端变为蓝色.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把pH=2的甲酸溶液稀释100倍后pH=3.5 | |
| B. | 0.1 mol•L-1的甲酸溶液的pH约为2 | |
| C. | HCOONa溶液能使酚酞试液变红 | |
| D. | 50mL l mol•L-1的甲酸溶液恰好与50mL l mol•L-1的NaOH溶液完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不能让小学生咬铅笔头,否则会引起铅中毒 | |
| B. | 食用碱用于面包加工,可以使面包疏松 | |
| C. | 铝合金用作门窗框架,这是利用了合金硬度大的特征 | |
| D. | 烧碱和冰醋酸均为电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com