
【题目】100℃时,Kw=1×10-12,对纯水的叙述正确的是
A. pH=6显弱酸性 B. c(H+)=10-6 mol/L,溶液为中性
C. Kw是常温时的10-2倍 D. 常温下,pH=6的溶液为中性
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在实验室用如下装置制备氯气.请回答: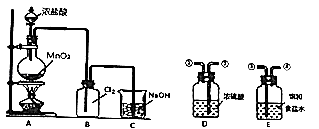
(1)写出A装置中制取氧气的化学方程式: M .
(2)若要制备纯净、干燥的氯气,需在A、B之间添加净化装置D、E,其中导管连接的顺序是(填写数字编号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】解释下列事实的方程式不正确的是( )
A.Al溶于NaOH溶液:2Al+2H2O+2NaOH═2NaAlO2+3H2↑
B.盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH﹣═SiO ![]() +H2O
+H2O
C.向FeCl3溶液中滴加淀粉碘化钾溶液,溶液变蓝:2Fe3++2I﹣═2Fe2++I2
D.红热的Fe丝与水接触,表面形成蓝黑色保护层:2Fe+3H2O(g) ![]() Fe2O3+3H2↑
Fe2O3+3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为清理路面积雪人们使用了一种融雪剂,其主要成分的化学式为XY2 , X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1mol XY2含有54mol电子.
(1)X元素在元素周期表中的位置 , 该融雪剂的化学式是 .
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是;D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8e﹣稳定结构,电子式为 .
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中加热时生成的产物的电子式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用如图所示的装置及药品进行比较酸性强弱的实验,一段时间后试管②中有胶冻状物质生成.下列说法正确的是( ) 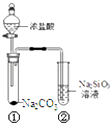
A.向Na2SiO3溶液中滴入酚酞溶液无明显现象
B.试管①中反应的离子方程式是:Na2CO3+2H+═2Na++CO2↑+H2O
C.该实验可以证明酸性:盐酸>碳酸>硅酸
D.若将盐酸换成硫酸,能证明酸性:硫酸>碳酸>硅酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2O2具有强氧化性,可以用来漂白纺织类物品、麦杆、纤维等.
(1)Na2O2中O元素的化合价为 .
(2)如图所示实验,滴入几滴水,现象是 , 反应的化学方程式为 . 实验结束后,向试管所得溶液中滴加酚酞溶液,现象是 .
(3)若用嘴通过导管向附着少量Na2O2粉末的棉花吹气,棉花燃烧.原因是Na2O2与H2O和CO2反应,其中与CO2反应的化学方程式为 . 若标准状况下反应生成了5.6L O2 , 则转移电子的物质的量为mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度为0.50mol/L的某金属阳离子Mn+的溶液10.00mL,恰好与0.4mol/L的NaOH溶液12.50 mL完全反应,生成沉淀,则n等于
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com