
在宏观—微观—符号之间建立联系,是化学学科特有的思维方式。汽车尾气是造成大气污染的主要原因之一,在汽车排气管上安装“催化转换器”便可以使汽车的尾气转换成无毒气体。如用 表示碳原子,用
表示碳原子,用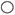 表示氧原子,用
表示氧原子,用 表示氮原子,下图为气体转换的微观过程。请你根据图示回答下列问题:
表示氮原子,下图为气体转换的微观过程。请你根据图示回答下列问题:
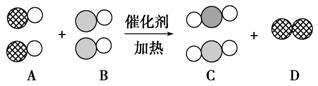
(1)A、B、C三种物质可以归为一类的依据是_____________________________________________________________
_________________________________________________________。
(2)将C归为化合物,将D归为单质的理由是_____________________________________________________________
_______________________________________________________。
(3)用化学反应方程式表示为_________________________________________________________________
_____ ____________________________________________________。
____________________________________________________。
化学变化过程中消耗的A物质和生成的C物质的质量比为____________。
(4)从微观的角度去描述你获得的关于化学变化的有关信息(答出一条即可)______________________________________________________。
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
利用X射线对BaSO4穿透能力较差的特性,医学上在进行消化系统的X射线透视时,常用BaSO4作内服造影剂,这种检查手段称为钡餐透视。
(1)医学上进行钡餐透视时为什么不用BaCO3?(用离子方程式表示)________________________________________________________________________。
(2)某课外活动小组为了探究BaSO4的溶解度,分别将足量BaSO4放入:
a.5 mL 水;
b.40 mL 0.2 mol/L 的Ba(OH)2溶液;
c.20 mL 0.5 mol/L的Na2SO4 溶液;
d.40 mL 0.1 mol/L 的H2SO4 溶液中,溶解至饱和。
①以上各溶液中,Ba2+的浓度由大到小的顺序为________。
A.b>a>c>d B.b>a>d>c
C.a>d>c>b D.a>b>d>c
②已知298 K时,Ksp(BaSO4)=1.1×10-10,上述条件下,溶液b中的SO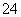 浓度为________ mol/L,溶液c中Ba2+的浓度为________ mol/L。
浓度为________ mol/L,溶液c中Ba2+的浓度为________ mol/L。
③某同学取同样体积的溶液b和溶液d直接混合,则混合液的pH为________(设混合溶液的体积为混合前两溶液的体积之和)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,可逆反应A(g)+3B(g) 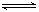 2C(g)达到平衡状态的标志是
2C(g)达到平衡状态的标志是
A. C生成的速率与A分解的速率2倍相等
B. 单位时间生成n mol A,同时生成3n mol B
C. A、B、C的浓度不再变化
D. A、B、C的分子数比为1∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
物质分类的依据通常有组成和性质。下列物质分类中,只考虑组成的是
A.Na2SO4是钠盐、硫酸盐、正盐
B.HNO3是一元酸、强酸、挥发性酸
C.Mg(OH)2是二元碱、难溶性碱、中强碱
D.Al2O3是两性氧化物、金属氧化物、最高价氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中属于纯净物的是
①由同种元素组成的物质 ②具有固定熔沸点的物质 ③由相同种类和相同数目的原子组成的分子 ④只有一种元素的阳离子和另一种元素的阴离子组成的物质 ⑤在氧气中燃烧只生成二氧化碳的物质 ⑥只含有一种分子的物质
A.②③⑥ B.④⑤⑥
C.①④ D.②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
取碘水四份于试管中,编号为Ⅰ、Ⅱ、Ⅲ、Ⅳ,分别加入汽油、CCl4、酒精、NaCl溶液,振荡后静置,现象正确的是( )
A.Ⅰ中溶液分层,下层呈紫红色
B.Ⅱ中溶液分层,下层呈紫红色
C.Ⅲ中溶液分层,下层呈棕黄色
D.Ⅳ中溶液不分层,溶液由棕黄色变成黄绿色
查看答案和解析>>
科目:高中化学 来源: 题型:
氢氧燃料电池以KOH溶液为电解质溶液,下列有关该电池的叙述不正确的是
( )
A.正极反应式为:O2+2H2O+4e-===4OH-
B.工作一段时间后,电解液中KOH的物质的量浓度不变
C.该燃料电池的总反应方程式为:2H2+O2===2H2O
D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.4 mol 电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
为节省药品和时间,甲、乙、丙三位同学用铜片、锌片、稀硫酸、CuSO4溶液、直流电源、石墨电极、导线、烧杯、试管等中学化学常见的药品和仪器(用品),通过巧妙的构思,设计了比较铜、锌金属活动 性相对强弱的系列实验。试填写下列空白:
性相对强弱的系列实验。试填写下列空白:
(1)甲同学分别将一小片铜片、锌片置于烧杯底部(铜与锌不接触),向烧杯中小心加入稀硫酸,观察到的现象是________。甲同学的设计思路是_____________________________。
(2)乙同学接着甲的实验,向烧杯中滴加________溶液,进而观察到的现象是____________________________________________________________ ____________。
____________。
乙同学作出锌、铜金属活动性相对强弱的结论所依据的原理是____________________________________________________________________。
(3)丙同学使用直流电源、石墨电极组装好电解装置,向乙同学实验后的溶液中补充了必要的试剂________ 溶液(作为电解液)。反应在调控下随即开始,实验中有关反应的化学方程式为________________________。实验中的明显现象是____ ____________________。
____________________。
(4)请你再单独设计一个简单的实验(试剂、仪器自选),探究和证实锌、铜金属活动性的相对强弱(简要说明操作和现象)______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解尿素[CO(NH2)2]的碱性溶液制氢,装置如下图所示,电解池中的隔膜仅阻止气体通过。电解时总的化学方程式为:
CO(NH2)2+2OH-通电CO32-+N2↑+3H2↑
以下说法不正确的是
A.a为阳极,b为阴极
B.电解时,溶液中OH—向b极移动
C.阴极反应式:2H2O+2e-===H2↑+2OH-
D.电解后,溶液pH减小

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com