

 .
.分析 (1)结合常见的烃基、官能团的名称和结构简式判断;
(2)烷烃的通式为CnH2n+2,根据相对分子质量可知12n+2n+2=72,则n=5,该烷烃的分子式应为C5H12,跟氯气反应生成的一氯代物只有一种,说明结构对称,分子中只含有一种H;
(3)由名称可确定主链碳原子数以及烃基的种类和位置,可写成结构简式.
解答 解:(1)-CH2CH3为乙基,-OH 为羟基,碳碳双键为 ,故答案为:乙基;羟基;
,故答案为:乙基;羟基; ;
;
(2)烷烃的通式CnH2n+2,该烷烃的相对分子质量为72,所以有:12n+2n+2=72,即14n=70,解得n=5,即分子式为C5H12.
含5个碳原子的烷烃的一氯取代物只有一种,说明烃分子中12个氢原子的位置均是等效的,分子结构对称,结构简式应为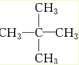 ,
,
故答案为: ;
;
(3)4,4,5-三甲基-2-己炔,该有机物主链为己炔,碳碳三键在2号C,在4、4、5号C原则各含有1个甲基,该有机物的结构简式为:CH3C≡C-C(CH3)2CH(CH3)2,2,2-二甲基-3-乙基-4-异丙基壬烷,主链为壬烷,含有9个C,在2号C含有2个甲基、在3号C含有1个乙基、在4号C含有1个异丙基,该有机物的结构简式为:CH3C(CH3)2CH(C2H5)CH(CCH3CH3)CH2CH2CH2CH2CH3,
故答案为:?CH3C≡C-C(CH3)2CH(CH3)2;?CH3C(CH3)2CH(C2H5)CH(CCH3CH3)CH2CH2CH2CH2CH3.
点评 本题考查较为综合,涉及有机物的组成、结构以及命名,为高频考点,侧重于双基的考查,有利于培养学生良好的科学素养,注意相关基础知识的积累,难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
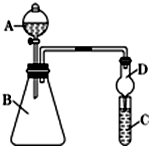 小明和同班同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
小明和同班同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 为了充分应用资源,用工业废碱液(Ca(OH)2、NaOH)与烟道气(回收成份SO2)来制取石膏(CaSO4•2H2O)和过二硫酸钠(Na2S2O8).设计简要流程如下:
为了充分应用资源,用工业废碱液(Ca(OH)2、NaOH)与烟道气(回收成份SO2)来制取石膏(CaSO4•2H2O)和过二硫酸钠(Na2S2O8).设计简要流程如下: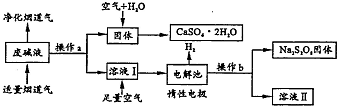
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
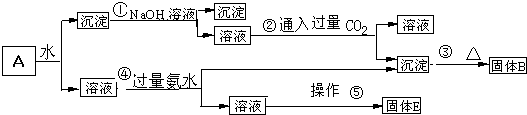
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
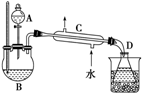 乙醇的沸点是78℃,能与水以任意比混溶,易与氯化钙结合生成配合物.乙醚的沸点为34,.6℃,难溶于水,乙醚极易燃烧.实验室制乙醚的反应原理是2CH3CH2OH$→_{140℃}^{浓H_{2}SO_{4}}$CH3CH2-O-CH2CH3(乙醚)+H2O
乙醇的沸点是78℃,能与水以任意比混溶,易与氯化钙结合生成配合物.乙醚的沸点为34,.6℃,难溶于水,乙醚极易燃烧.实验室制乙醚的反应原理是2CH3CH2OH$→_{140℃}^{浓H_{2}SO_{4}}$CH3CH2-O-CH2CH3(乙醚)+H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题
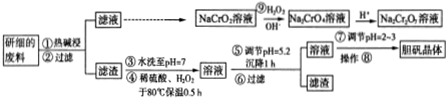
| 沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 | Fe(OH)2 |
| pH | 2.9 | 6.7 | 9.4 | 9.7 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、蛋白质、油脂均是天然高分子化合物 | |
| B. | 铜矿石在细菌作用下可直接转化为单质铜,这个过程叫生物炼铜 | |
| C. | 氟氯烃的肆意排放会加速臭氧层的破坏,使大气层中的紫外线增强 | |
| D. | 凯库勒的“基团理论”尽管存在缺陷,但仍对有机化学的发展起到了巨大的推动作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com