
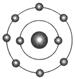
 。下列原子中,与氟元素原子的化学性质相似的是( )
。下列原子中,与氟元素原子的化学性质相似的是( )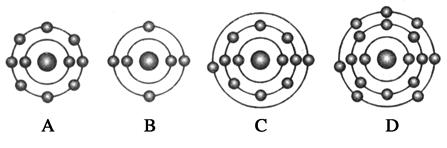
科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.②③④ | C.②④⑤ | D.①③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.它们的原子最外层电子数相等,元素的最高正化合价都是+5 |
| B.氮的非金属性比砷强,所以NH3的稳定性大于AsH3 |
| C.因为氮的原子半径比砷的小,所以氮的相对原子质量比砷的相对原子质量小 |
| D.它们都是主族元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大 |
| B.元素X不能与元素Y形成化合物X2Y2 |
| C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR |
| D.元素W、R的最高价氧化物对应的水化物都是强酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.某原子K层上只有一个电子 |
| B.某原子M层上的电子数为L层上电子数的4倍 |
| C.某离子M层上和L层上的电子数均为K层的4倍 |
| D.某离子的核电荷数与最外层电子数相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素半径大小呈周期性变化 | B.元素相对质量依次递增 |
| C.元素核外电子排布呈周期性变化 | D.元素最高正化合价呈周期性变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com