
【题目】下列有关甲烷的说法中错误的是 ( )
A.采煤矿井中的甲烷气体是植物残体经微生物发酵而来的
B.天然气的主要成分是甲烷
C.甲烷是没有颜色、没有气味的气体,极易溶于水
D.甲烷与氯气发生取代反应所生成的产物四氯甲烷是一种效率较高的灭火剂
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
【题目】(1)A图是“四种基本反应类型与氧化还原反应的关系”图,请在A图中用阴影部分表示反应:H2+CuO![]() Cu+H2O所属的区域。
Cu+H2O所属的区域。
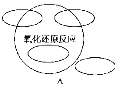
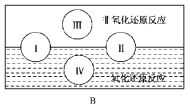
(2)“四种基本反应类型与氧化还原反应的关系”也可用B图表达。其中Ⅰ为化合反应,则Ⅱ为________反应。写出有水生成的符合反应类型Ⅲ的一个化学方程式:____________________。写出有水参加的符合反应类型Ⅳ的一个化学方程式_____________,其中水________(填“被氧化”或“被还原”或“既被氧化又被还原”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式书写不正确的是( )
A. H2SO4=2H++SO42- B. NaHCO3=Na++H++CO32-
C. FeCl3=Fe3++3Cl- D. Ba(OH)2=Ba2++2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s)+ 3C(s)=2Fe(s)+ 3CO(g)ΔH 1=+489.0 kJ·mol-1,
C(s)+CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为 。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式: 。
(3)一定温度下,在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
①CO的平衡转化率(α)与温度、压强的关系如下图所示。

B、C两点的平衡常数K(B) K(C)(填“>”、“=”或“<”).
②某温度下,将2.0molCO和6.0molH2充入2L的密闭容器中,达到平衡时测得c(CO)=0.25mol/L,CO的转化率= ,此温度下的平衡常数K= (保留二位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素的激发态原子的电子排布式为1s22s22p63s23p34s1 , 则该元素基态原子的电子排布式为;元素符号为;其最高价氧化物对应的水化物的化学式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”简化表示.
CH3﹣CH═CH﹣CH3可简写为![]() .
.
(1)有机物X的键线式为: ,该有机物与H2加成时最多能消耗氢气的物质的量 ,有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式 ,将Y加入酸性高锰酸钾溶液中的现象 .
,该有机物与H2加成时最多能消耗氢气的物质的量 ,有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式 ,将Y加入酸性高锰酸钾溶液中的现象 .
(2)Y与乙烯在一定条件下发生等物质的量聚合反应,写出其反应的化学方程式: .
(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有 种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学平衡常数的说法中,正确的是( )
A.在任何条件下,化学平衡常数都是一个定值
B.化学平衡常数K可以推断一个可逆反应进行的程度
C.化学平衡常数K只与温度、反应物浓度、体系的压强有关
D.当改变反应物的浓度时,化学平衡常数会发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知环戊烯结构简式为![]() 可简写为
可简写为![]() 降冰片烯的分子结构可表示为:
降冰片烯的分子结构可表示为:
(1)降冰片烯属于
A.环烃 B.不饱和烃 C.烷烃 D.芳香烃
(2)降冰片烯的分子式为 ;
(3)降冰片烯不具有的性质
A.能溶于水 B.发生氧化反应 C.加成反应 D.常温常压下为气体
(4)写出环戊烯发生加聚反应的化学方程式 ;
(5)实验室制取乙炔的化学方程式: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com