
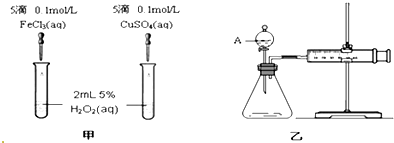
分析 (1)①根据H2O2分解的催化作用有可能是氯离子起的作用解答即可;
②根据乙图装置来选择气密性的检查方法,该反应是通过反应速率分析的,所以根据v=$\frac{△c}{△t}$来判断;
(2)①此反应的反应物为酸性高锰酸钾和草酸溶液,生成物突然无色,说明生成锰离子,依据氧化还原反应原理书写化学反应方程式即可;
②锰离子有催化作用;要想验证锰离子的催化作用,再加入硫酸锰即可;
(3)根据KI、Na2S2O3与淀粉的反应原理解答.
解答 解:(1)①由于两种催化剂的阴离子与阳离子均不同,故阴离子也可能对双氧水的分解起到催化作用,
故答案为:否;两催化剂的阴离子不同;
②结合乙图装置,该气密性的检查方法为:关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,如活塞复原,则装置的气密性良好;反应是通过反应速率分析的,根据v=$\frac{△c}{△t}$,所以,实验中需要测量的数据产生40ml气体所需的反应时间,
故答案为:关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,如活塞复原,则装置的气密性良好;产生40ml气体所需的反应时间;
(2)①酸性高锰酸钾和草酸溶液在硫酸酸化条件下生成硫酸锰、硫酸钾等,化学反应方程式为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,
故答案为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑;
②KMnO4与H2C2O4反应生成硫酸锰,锰离子有催化作用,所以猜想还可能是催化剂的作用,要想验证锰离子的催化作用,在做对比实验时同时加入硫酸锰观察反应速率是否变化即可,
故答案为:催化剂;B;
(3)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,先发生S2O82-+2I-═2SO42-+I2(慢),后发生I2+2S2O32-═S4O62-+2I- (快),当S2O32-耗尽后,碘才能与淀粉作用显示蓝色,用淀粉溶液做指示剂,通过褪色时间判断浓度与反应速率的关系,I2应完全反应,蓝色褪去,采取控制变量法,KI的浓度不变,改变K2S2O8溶液浓度,即采取①④⑤或②④⑤,S2O82-+2I-═2SO42-+I2 (慢) I2+2S2O32-═2I-+S4O62-(快),当有蓝色出现时,快反应进行完全,
此时只发生反应:S2O82-+2I-═2SO42-+I2 (慢)
1 1
故有I2+2S2O32-═2I-+S4O62-(快),
1 2
c $\frac{4.0×1{0}^{-3}L×0.10mol•{L}^{-1}}{(4+4+1+1)×1{0}^{-3}L}$=0.04mol/L,
故△c(I2)=△c(S2O82-)=0.02mol/L,故v(S2O82-)=$\frac{0.02mol•{L}^{-1}}{2s}$=0.01mol•L-1•s-1,
故答案为:Na2S2O3;①④⑤或②④⑤;0.01mol•L-1•s-1.
点评 本题考查了实验探究,注意探究外界条件对化学反应影响时,只能改变一个条件,其它条件必须相同,否则不能得出正确结论,化学反应速率的计算难度较大,注意反应关系和溶液的总体积.


科目:高中化学 来源: 题型:选择题
| A. | v(A2)=0.8 mol•L-1•s-1 | B. | v(A2)=30 mol•L-1•min-1 | ||
| C. | v(AB3)=1.0 mol•L-1•s-1 | D. | v(B2)=1.2 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaOH固体 | B. | 水 | C. | CuSO4固体 | D. | 氯化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
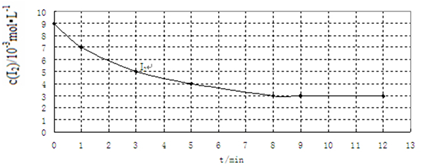
| 实验 编号 | 实验目的 | 温度/℃ | 催化剂 质量/g | 反应物初始浓度 /10-3mol•L-1 | |
| H2 | I2 | ||||
| Ⅰ | 为以下实验作参照 | 457 | 0 | 7 | 9 |
| Ⅱ | 420 | 7 | 9 | ||
| Ⅲ | 探究催化剂对该反应速率的影响 | 10 | 7 | 9 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
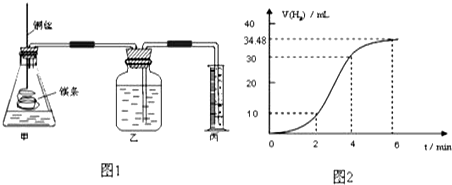
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 10%H2O2的体积/mL | 5.0 | 5.0 | V1 | V2 |
| 20%硫酸的体积/mL | 0 | 0.5 | 1.0 | V3 |
| 水的体积/mL | 15 | 14.5 | V4 | 13.5 |
| 所需时间t/s | t1 | t2 | t3 | t4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
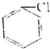 ②
② ③(CH3)3CCH2Cl ④CHCl-CHBr2⑤
③(CH3)3CCH2Cl ④CHCl-CHBr2⑤ ⑥CH3Cl.
⑥CH3Cl.| A. | ②③⑤ | B. | ①③⑥ | C. | 全部 | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 正极 | Fe | Fe | C | Cu |
| 负极 | Cu | Zn | Fe | Zn |
| 电解质溶液 | HCl | CuSO4 | CuSO4 | FeSO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com