
下列说法中正确的是
A.在铁质船体上镶嵌锌块,可以减缓船体被海水腐蚀的速率
B.粗铜精炼时,电镀液中的c(Cu2+)保持不变
C.纯银在空气中久置变黑发生的是电化学腐蚀
D.外加电流的阴极保护法是将被保护的金属与外加电源的正极相连
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列反应所产生的气体体积在标准状况下为22.4 L的是( )
A.将2 mol金属Cu与含2 mol H2SO4的浓硫酸共热
B.将27 g Al与足量 盐酸反应
盐酸反应
C.常温下,将18 g金属铝投入足量NaOH溶液中
D.常温下,将10.8 g Al和22.4 g Fe投入到300 g 98%的硫酸中
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒夏特列原理解释的是( )
A.红棕色NO2加压后颜色先变深后变浅
B.实验室中常用排饱和食盐水的方法收集氯气
C.SO2催化氧化成SO3的反应,使用过量的空气以提高二氧化硫的利用率
D.压缩H2与I2(g)反应的平衡混合气体,颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
关于下列装置说法正解的是( )
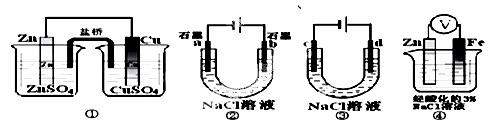
A.装置①中,盐桥中的Cl-移向CuSO4溶液
B.装置②工作一段时间后,a极附近溶液的pH降低
C.用装置③精炼铜时,c极为粗铜
D.装置④中电子由Zn流向Fe,Zn极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
I、恒温下,将a mol N2与b mol H2的混合气体通入一个固体容积的密闭容器中,发生如下反应:N2(g)+3H2(g)  2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,nt(N2)=13 mol,nt(NH3)=6 mol,计算 a= 。
(2)反应达到平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量 。。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),
n( 始):n(平)= 。
(4)原混合气体中,a:b= 。
(5)达到平衡时,N2和H2的转化率之比,a(N2):a(H2)= 。
(6)平衡混合气体中,n(N2):n(H2):n(NH3)= 。
II、若向体积不变的密闭容器中充入2 mol N2和6 mol H2,一定条件下发生反应:
N2(g)+ 3 H2(g) 2 NH3(g),平衡时混合气共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
2 NH3(g),平衡时混合气共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
(1)若a=0,b=0,则c= .
(2)若a=0.7,b=2.1,则:
① c= .
②这时反应向 进行,因为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
氮氧化铝(AlON)是一种透明高硬度防弹材料,可以由反应Al2O3+C+N2=2AlON+CO(高温)合成,下列有关说法正确的是
A.氮氧化铝中氮的化合价是-3
B.反应中氮气作氧化剂
C.反应中每生成5.7g AlON 同时生成1.12 L CO
D.反应中氧化产物和还原产物的物质的量之比是2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
Q、W、X、Y、Z为五种原子序数依次增大的短周期元素。已知:
①Q原子的核外电子数等于电子层数,且与W组成的一种化合物是沼气的主要成分;
②元素X的最高价氧化物的水化物和其气态氢化物能够反应,生成离子化合物甲;
③W与Y组成的化合物乙,是机动车排出的大气污染物之一,也是造成“雾霾”天气的有害物质之一;
④Y与Z能形成电子总数为30和38的两种离子化合物,分别为丙和丁
(1)W在周期表中的位置是_______________;
丁的电子式是 ____ _______。
(2)WY2与Z2Y2反应的化学方程式是__________________。
(3)甲在水溶液中的水解方程式为_______________
(4)写出一种实验室制取XQ3的方法____________(用化学方程式表示)
(5)标准状况下22.4L X的气态氢化物,与0.5L 1mol/L的X最高价氧化物的水化物反应,所得溶液中离子浓度由大到小的顺序是__________(用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
空气中的自由电子附着在分子或原子上形成的空气负离子(也叫阴离子)被称为“空气维生素”。O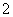 就是一种空气负离子,其摩尔质量为( )
就是一种空气负离子,其摩尔质量为( )
A.32 g B.33 g
C.32 g·mol-1 D.33 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
A.用氢氧化钠溶液吸收二氧化氮:2OH-+2NO2===NO +NO↑+H2O
+NO↑+H2O
B.碳酸氢钠溶液与过量的澄清石灰水反应:2HCO +Ca2++2OH-===CaCO3↓+CO
+Ca2++2OH-===CaCO3↓+CO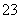 +2H2O
+2H2O
C.用浓盐酸酸化的KMnO4溶液与H2O2反应:2MnO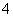 +6H++5H2O2===2Mn2++5O2↑+8H2O
+6H++5H2O2===2Mn2++5O2↑+8H2O
D.硫酸氢钠溶液与足量氢氧化钡溶液混合:H++SO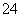 +Ba2++OH-===BaSO4↓+H2O
+Ba2++OH-===BaSO4↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com