
【题目】亚氯酸钠(NaClO2)用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点.其在溶液中可生成ClO2、HClO2、ClO2﹣、Cl﹣等,其中HClO2和ClO2都具有漂白作用.已知pOH=﹣lgc(OH﹣),经测定25℃时各组分含量随pOH变化情况如图所示(Cl﹣没有画出),此温度下,下列分析错误的是( ) 
A.HClO2的电离平衡常数的数值Ka=10﹣6
B.亚氯酸钠在碱性条件下较稳定
C.pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2﹣)>c( ClO2)>c( Cl﹣)
D.同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有c(HClO2)+2c(H+)=c(ClO2﹣)+2c(OH﹣)
【答案】C
【解析】A、HClO2的电离平衡常数K=  ,观察图象可以看出,当pOH=8时,pH=6,c(ClO2﹣)=c(HClO2),因此HClO2的电离平衡常数的数值Ka=10﹣6 , 故A正确;
,观察图象可以看出,当pOH=8时,pH=6,c(ClO2﹣)=c(HClO2),因此HClO2的电离平衡常数的数值Ka=10﹣6 , 故A正确;
B、由图可以得出:碱性条件下ClO2﹣浓度高,即在碱性条件下亚氯酸钠较稳定,故B正确;
C、根据图知,pH=7时,存在c(HClO2)<c( ClO2﹣),则微粒浓度大小顺序是c( ClO2﹣)>c(HClO2)>c( ClO2)>c( Cl﹣),故C错误;
D、依据电中性原则得出:c(H+)+c(Na+)=c(ClO2﹣)+c(OH﹣)+c(Cl﹣) ①,依据物料守恒得出:2c(Na+)=c(ClO2﹣)+c(HClO2)+(ClO2)+c(Cl﹣) ②,联立①②消去钠离子:c(HClO2)+2c(H+)=c(ClO2﹣)+2c(OH﹣),故D正确;
故选C.
A、HClO2的电离平衡常数K=  结合图示数据来计算;
结合图示数据来计算;
B、由图可以得出:碱性条件下ClO2﹣浓度高;
C、根据图知,pH=7时,c(HClO2)<c( ClO2﹣);
D、依据电中性原则得出:c(H+)+c(Na+)=c(ClO2﹣)+c(OH﹣)+c(Cl﹣),依据物料守恒得出:2c(Na+)=c(ClO2﹣)+c(HClO2)+(ClO2)+c(Cl﹣),据此解答即可.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体,化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①式化工生产中的一种重要固氮反应. 请回答下列问题: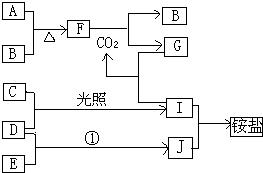
(1)、 A、B、C、D、E、F、G、I、J各为什么物质?
(2)写出下列物质间反应的化学方程式:A和B,F和CO2 , D和E,I和J.
(3)写出化合物G与I反应的离子方程式.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于油脂的结构 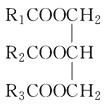 的说法正确的是( )
的说法正确的是( )
A.油脂是高级脂肪酸与甘油生成的酯
B.若R1、R2、R3都是饱和烃基,称为简单甘油酯
C.若R1、R2、R3都是不饱和烃基,称为混合甘油酯
D.某油脂分子中,所含烃基有三种,但每一个油脂分子中所含这三种烃基都相同,而且排列结构也相同,则该油脂为混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】基态原子的核外电子排布为[Kr]4d105s1的元素属于的区、周期和族为
A. p区、第五周期、ⅠB族 B. ds区、第五周期、ⅠB族
C. d区、第四周期、ⅠB族 D. ds区、第五周期、Ⅷ族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据最近的美国《农业研究》杂志报道,美国科学家发现半胱氨酸能增强艾滋病病毒感染者的免疫力,对控制艾滋病病毒的蔓延有奇效。已知半胱氨酸的结构简式为 ![]() ,则下列说法不正确的是( )
,则下列说法不正确的是( )
A.半胱氨酸属于α氨基酸
B.半胱氨酸是一种两性化合物
C.两分子半胱氨酸脱水形成的二肽的结构简式为
D. 与NaOH溶液加热时可放出一种碱性气体
与NaOH溶液加热时可放出一种碱性气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B两种有机物的分子式相同,都可用CaHbOcNd表示,且a+c=b , a-c=d。已知A是天然蛋白质水解的最终产物;B是一种含有醛基的硝酸酯。试回答:
(1)A和B的分子式是。
(2)光谱测定显示,A的分子结构中不存在甲基,则A的结构简式为。
(3)光谱测定显示,B的烃基中没有支链,则B的结构简式为。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com