
【题目】糖尿病是由于体内胰岛素紊乱导致的代谢紊乱综合症,以高血糖为主要标志,长期摄入高热量食品和缺少运动都易导致糖尿病。
(1)血糖是指血液中的葡萄糖(C6H12O6),下列说法正确的是_________(错选倒扣分)。
A.葡萄糖属于碳水化合物,分子可表示为 C6(H2O)6,则每个葡萄糖分子中含6个H2O
B.糖尿病人尿糖也高,可用新制的氢氧化铜悬浊液来检测病人尿液中的葡萄糖
C.葡萄糖可用于制镜工业
D.淀粉水解的最终产物是葡萄糖
(2)木糖醇[CH2OH(CHOH)3CH2OH]是一种甜味剂,糖尿病人食用后不会升高血糖,请预测木糖醇的一种化学性质:_________;
(3)糖尿病人不可饮酒,酒精在肝脏内可被转化成有机物 A,A 的实验结果如下:
Ⅰ.通过样品的质谱测得 A 的相对分子质量为 60
Ⅱ.核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目,例如:乙醇(CH3CH2OH) 有三种氢原子(图1),经测定,有机物 A 的核磁共振氢谱示意图如图:
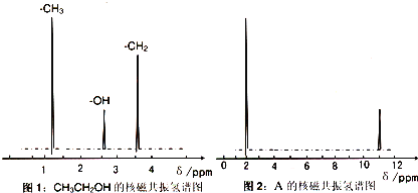
Ⅲ.将 A 溶于水,滴入石蕊试液,发现溶液变红,试推导写出 A 的结构简式为________ ;
(4)糖尿病人宜多吃蔬菜和豆类食品.蔬菜中富含纤维素,豆类食品中富含蛋白质,下列说法错误的是:_________(填序号,错选倒扣分);
A.蛋白质都属于天然有机高分子化合物,蛋白质都不溶于水
B.用灼烧闻气味的方法可以区别合成纤维和羊毛
C.人体内不含纤维素水解酶,人不能消化纤维素,因此蔬菜中的纤维素对人没有用处
D.紫外线、医用酒精能杀菌消毒,是因为使细菌的蛋白质变性
E.用天然彩棉制成贴身衣物可减少染料对人体的副作用
(5)香蕉属于高糖水果,糖尿病人不宜食用.乙烯是香蕉的催熟剂,可使溴的四氯化碳溶液褪色,试写出该反应的化学方程式:_________。
【答案】BCD 能与羧酸发生酯化反应 CH3COOH AC CH2=CH2+Br2→CH2Br﹣CH2Br
【解析】
(1)A、葡萄糖的化学式为C6H12O6,不含有水,故A错误;
B、葡萄糖中含有醛基,醛基能与新制的氢氧化铜反应生成砖红色沉淀,故B正确;
C、葡萄糖中含有醛基,能发生银镜反应,故C正确;
D、淀粉水解最终生成葡萄糖,故D正确;
(2)木糖醇中含有羟基,羟基能发生酯化反应;
(3)核磁共振氢谱中有几个峰就有几种氢原子,图2有2个峰,说明有2种氢原子,A 溶于水,滴入石蕊试液,发现溶液变红,溶液呈酸性,说明含有羧基,根据相对分子质量为60,60﹣45=15,另一个基团为甲基,A为CH3COOH;
(4)A、蛋白质均属于天然高分子化合物,它们的相对分子质量在10000万以上,部分蛋白质可溶于水,如血清蛋白、酶等,故A说法错误;
B、羊毛是蛋白质,因蛋白质灼烧时有烧焦羽毛的特殊气味,所以可用灼烧来鉴别合成纤维和羊毛,故B说法正确;
C、人类膳食中的纤维素主要含于蔬菜和粗加工的谷类中,虽然不能被消化吸收,但有促进肠道蠕动,利于粪便排出等功能,故C说法错误;
D、细菌的成分是蛋白质,紫外线、医用酒精能使蛋白质变性,能杀菌消毒,故D说法正确;
E、天然彩棉对人体无不良反应,用天然彩棉制成贴身衣物可减少染料对人体的副作用,故E说法正确;
(5)乙烯含有碳碳双键,与溴发生加成反应,生成1,2﹣二溴乙烷,使溴的四氯化碳溶液褪色,反应生成1,2﹣二溴乙烷,反应方程式为CH2=CH2+Br2→CH2Br﹣CH2Br。


 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】以乙醇为主要原料合成一种具有果香味的物质 C 和化合物 D 的合成路线如图所示。
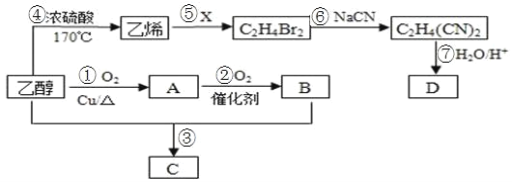
请回答下列问题:
(1)B的结构简式为_______。
(2)反应⑤的化学方程式为_______;B分子中的官能团名称为_______;反应⑥的类型为________。
(3)为了探究反应③的反应原理,通常采用“同位素示踪法”的方法,请结构简式为 CH3CH218OH,书写化反应③学方程式为_______。
(4)已知D的相对分子量为 118,其中碳、氢两元素的质量分数分别为 40.68%、5.08%,其余为氧元素,则 D 的分子式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液体燃料电池相比于气体燃料电池具有体积小等优点。一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是
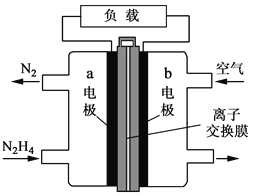
A. b极发生氧化反应
B. a极的反应式:N2H4+4OH--4e-=N2↑+4H2O
C. 放电时,电流从a极经过负载流向b极
D. 其中的离子交换膜需选用阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】VA族的氮、磷、砷(As)等元素的化合物在科研和生产中有许多重要用途,请回答下列问题。
(1)砷的基态原子的电子排布式为___________________。
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为______________。
(3)NH3的沸点比PH3高,原因是___________;PO43-离子的立体构型为___________。
(4)AsH3是无色稍有大蒜气味的气体,在AsH3中As原子的杂化轨道类型为______________。
(5)H3AsO4和H3AsO3是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比H3AsO3 酸性强的原因_____________________。
(6)磷的一种单质白磷(P4)属于分子晶体,其晶胞结构如下图。已知最近两个白磷分子间的距离为 a pm(1pm=10-12m),阿伏加德罗常数的值为NA,则该晶体的密度为__________________g/cm3(只要求列算式,不必计算)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备乙酸乙酯的绿色合成路线之一为:
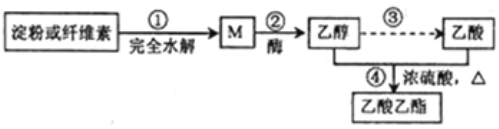
下列说法不正确的是( )
A. 加热条件下,M能与新制氢氧化铜悬浊液发生反应
B. ④的反应类型属于酯化反应,也属于取代反应
C. 淀粉和纤维素的化学式均为(C6H10O5)n,二者互为同分异构体
D. 用饱和碳酸钠溶液可以鉴别乙醇、乙酸和乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组设计了如下3个实验方案,用以检验淀粉的水解程度:
(1)甲方案:淀粉液![]() 水解液
水解液![]() 中和液
中和液![]() 溶液变蓝
溶液变蓝
结论:淀粉尚未水解。
(2)乙方案:淀粉液![]() 水解液
水解液![]() 无银镜现象
无银镜现象
结论:淀粉尚未水解。
(3)丙方案:

结论:淀粉水解完全。
上述三个方案操作是否正确?说明理由。_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铵被广泛用于医药、干电池、织物印染、洗涤等领域。氯化铵T1温度下有以下平衡:![]()
(1)N原子最外层电子有______种运动状态;上述平衡中物质,在晶体时属于离子晶体的是__________。
(2)![]() 的电子式为______________。
的电子式为______________。
(3)Cl的非金属性强于S,用原子结构的知识说明理由:_________________。
(4)上述该反应的平衡常数表达式为____________________________________。
(5)在2L密闭容器中建立平衡,不同温度下氨气浓度变化正确的是_________。

(6)T1温度在2L,容器中,当平衡时测得![]() 为amol/L,保持其他条件不变,压缩容器体积至1L(各物质状态不变),重新达到平衡后测得
为amol/L,保持其他条件不变,压缩容器体积至1L(各物质状态不变),重新达到平衡后测得![]() 为bmol/L。试比较a与b的大小a_____b(填“>”“<”或“=”),并说明理由:___________。
为bmol/L。试比较a与b的大小a_____b(填“>”“<”或“=”),并说明理由:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的结构与性质之间有密切的关系。请回答下列问题:
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于________晶体;Ni原子和C原子之间存在________键。
(2)很多不饱和有机物在Ni催化下可以与H2发生加成反应。如①CH2=CH2、②CH≡CH、③HCHO等,这些分子中C原子为sp2杂化的有________(填物质序号)。
(3)已知苯酚(![]() )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子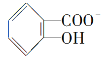 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)________Ka(苯酚)(填“>”或“<”),其原因是_____________。
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)________Ka(苯酚)(填“>”或“<”),其原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学向SO2和Cl2的混合气体中加入品红溶液,振荡,溶液褪色,将此无色溶液分成三份,依次进行实验,实验操作和实验现象记录如下:
序号 | |||
实验操作 |
|
|
|
实验现象 | 溶液不变红,试纸不变蓝 | 溶液不变红,试纸褪色 | 生成白色沉淀 |
下列实验分析中,不正确的是
A. ①说明Cl2被完全消耗
B. ②中试纸褪色的原因是:SO2 + I2 + 2H2O == H2SO4 + 2HI
C. ③中若将BaCl2溶液换成Ba(NO3)2溶液,也能说明SO2被Cl2氧化为SO42
D. 实验条件下,品红溶液和SO2均被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com