
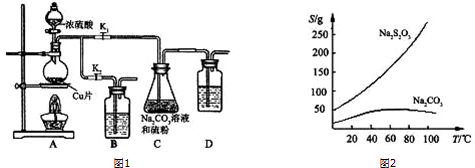
分析 在加热条件下,铜和浓硫酸发生氧化还原反应生成二氧化硫,所以A中发生的反应为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑;打开K1,关闭K2,在C中Na2CO3和S、SO2反应生成Na2S2O3,Na2S2O3溶液具有弱碱性和较强的还原性,所以酸性条件下不能存在,二氧化硫不能完全反应且二氧化硫有毒,会污染空气,所以用NaOH吸收未反应的SO2;C中溶液的pH接近7时即停止C中的反应,打开K2,关闭K1,二氧化硫有毒,应该用B中溶液吸收二氧化硫,二氧化硫属于酸性氧化物,且有还原性,所以可以碱性物质或氧化性物质吸收二氧化硫,
(1)铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水;根据题目Na2S2O3在酸性溶液中不能稳定存在的信息判断;二氧化硫不能排放到空气中,应有尾气处理装置;从滤液中获取Na2S2O3•5H2O需蒸发浓缩冷却结晶等操作;
(2)氯水中氯气和水反应生成盐酸和次氯酸,氯水中一定有氯离子;
(3)根据反应方程式中各物质计量数之间的关系求算.
解答 解:(1)铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑;由于Na2S2O3在酸性溶液中不能稳定存在,碳酸钠的作用是起反应物作用及提供碱性环境,所以当C中溶液的pH接近7时,打开K2、关闭K1并停止加热;SO2是大气污染物,需要尾气处理,则装置B、D中应盛放氢氧化钠溶液,用来吸收SO2,防止污染环境;Na2S2O3•5H2O受热易分解,所需冷却结晶,所以从滤液中获取Na2S2O3•5H2O需蒸发浓缩冷却结晶等操作,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑;接近7;Na2S2O3在酸性溶液中不能稳定存在;吸收SO2,防止污染;蒸发浓缩;冷却结晶;
(2)因为氯水中氯气和水反应生成盐酸和次氯酸,氯水中一定有氯离子,所以加入硝酸银生成沉淀,不能证明因Na2S2O3具有还原性,氯离子是氯气做氧化剂生成的,
故答案为:不正确,因为氯水中含有Cl-;
(3)溶液中发生的反应为:2Ba2++Cr2O72-=2BaCrO4+2H+、Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O、I2+2S2O32-=2I-+S4O62-;
根据方程式列出各物质的关系为Ba2+~BaCrO4~$\frac{1}{2}$Cr2O72-~$\frac{3}{2}$I2~3S2O32-
1mol 3mol
则n(Ba2+)=3n(S2O32-)=$\frac{1}{3}$×0.0100mol•L-1×18.00×10-3 L=6×10-5mol,所以c(Ba2+)═$\frac{6×10{\;}^{-5}mol}{25.00×10{\;}^{-3}L}$=2.4×10-3mol•L-1,
故答案为:2.4×10-3 mol•L-1.
点评 本题考查了有关硫代硫酸钠的知识,理解工艺流程,掌握实验操作与设计及物质性质是解答的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | n=2 | |
| B. | 第一次达平衡时,反应消耗的A为0.7 mol | |
| C. | 充入氮气后,反应速率加快,平衡正向移动 | |
| D. | 正反应放热 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60% | B. | 40% | C. | 24% | D. | 4% |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
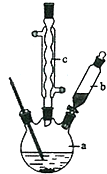 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线: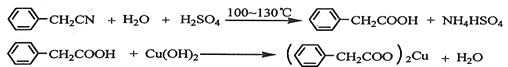
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡后CO的体积分数为40% | |
| B. | 平衡后CO的转化率为25% | |
| C. | 平衡后水的转化率为50% | |
| D. | 平衡后混合气体的平均相对分子质量为24 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com