
 某反应由两步反应A
某反应由两步反应A B
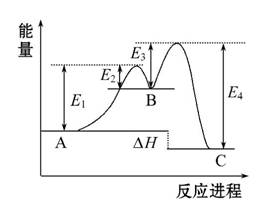
B C构成,它的反应能量曲线如右图(E1、E2、E3、E4表示活化能)。
C构成,它的反应能量曲线如右图(E1、E2、E3、E4表示活化能)。
下列有关叙述正确的是( )
A.两步反应均为吸热反应
B.三种化合物中C最稳定
C.加入催化剂会改变反应的焓变
D.整个反应的ΔH=E1-E2
科目:高中化学 来源: 题型:
某实验小组用铜绿[CuCO3·Cu(OH)2]、铁粉和稀硫酸制取铜,实验过程如下:加热铜绿得到一种黑色固体,将铁粉与稀硫酸反应制得的气体通入黑色固体中并加热,充分反应后得到铜。
(1)上述实验过程中所发生的化学方程式为:
______________________________________________________;
______________________________________________________;
______________________________________________________。
(2)某同学将上述实验过程改为:将铜绿溶于适量稀硫酸中,然后加入适量铁粉,充分反应后,过滤,也可以得到铜。则所发生的化学方程式为:
______________________________________________________;
______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于物质的分类正确的是( )
A.SO2、CO2、CO、NO2都是酸性氧化物
B.Na2O、Na2O2、Fe2O3、CuO都是碱性氧化物
C.HCl、HClO、HNO3、HClO4都是强酸
D.NaOH、KOH、Ba(OH)2、Ca(OH)2都是强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
下列的离子方程式中,书写正确的一项是( )
A.氨水中通入过量CO2:2NH3·H2O +CO2==== 2NH4++CO32-+H2O
B.稀硝酸中加入过量铁粉:3Fe + 8H++2 NO3-==== 3Fe2++ 2NO↑ + 4H2O
C.钠与水反应 Na+2H2O==== Na+ +2OH-+H2 ↑
D.Ca(ClO)2 溶液中通入过量的二氧化硫气体:ClO-+SO2+H2O==== HClO+HSO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知物质A、B、C、D、E、F在一定条件下的关系如下图所示,该六种物质的焰色反应均呈黄色。

(1)写出下列物质的化学式:A 、D 、F 。
(2)A、B、C、D四种物质分别长期暴露在空气中,其最终产物为 ,其中变质过程中有氧化还原反应发生的两种物质是(填写物质对应的化学式) 、 。
(3)将C加入CuSO4溶液中,发生反应的总化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
盖斯定律认为能量总是守恒的,不管化学反应过程是一步完成或分几步完成,整个过程的热效应是相同的。已知:
①H2O(g)====H2O(l) ΔH1=-Q1kJ·mol-1
②C2H5OH(g)====C2H5OH(l) ΔH2=-Q2kJ·mol-1
③C2H5OH(g)+3O2(g)====2CO2(g)+3H2O(g) ΔH3=- Q3kJ·mol-1
若使23 g液态无水酒精完全燃烧,最后恢复到室温,则放出的热量为(单位:kJ)( )
A.Q1+ Q2+ Q3 B.1.5Q1-0.5Q2+0.5Q3
C.0.5Q1-1.5Q2+0.5Q3 D.0.5(Q1+Q2+Q3)
查看答案和解析>>
科目:高中化学 来源: 题型:
依据元素周期表及元素周期律,下列推断正确的是( )
A.H3BO3的酸性比H2CO3的强
B.Mg(OH)2的碱性比Be(OH)2的强
C.HCl、HBr、HI的热 稳定性依次增强
稳定性依次增强
D.若M+和R2-的核外电子层结构相同,则原子序数:R>M
查看答案和解析>>
科目:高中化学 来源: 题型:
同周期元素W、X、Y、Z的原子序数依次增大,W、X原子的最外电子层电子数之比为4︰3,Z原子比X原子的核外电子数多4。下列说法正确的是 ( )
A. W、Y、Z的电负性大小顺序一定是Z>Y>W
B. W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z
C.Y、Z形成的分子的空间构型可能是正四面体
D.WY2分子中σ键与π键的数目之比是2︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:P4(s)+6Cl2(g)=4PCl3(g) ΔH=akJ·mol-1
P4(s)+10Cl2(g)=4PCl5(g) ΔH= bkJ·mol-1
P4具有正四面体结构,PCl5中P-Cl键的键能为ckJ·mol-1,PCl3中P-Cl键的键能为1.2ckJ·mol-1
下列叙述正确的是( )
A.P-P键的键能大于P-Cl键的键能
B.可求Cl2(g)+PCl3(g)=PCl5(s)的反应热ΔH
C.Cl-Cl键的键能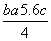 kJ·mol-1
kJ·mol-1
D.P-P键的键能为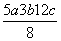 kJ·mol-1
kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com